Фармакодинамика
Противогрибковое средство. Производное триазола, проявляет противогрибковый эффект за счет блокады биосинтеза эргостерола клеточной мембраны грибов. «Мишень» для действия препарата — фермент 14-α-деметилаза.
14-α-деметилаза входит в группу ферментов, известных под общим названием цитохром Р450. Все ферменты группы цитохрома Р450 содержат гематиновый железосодержащий пигмент. Флуконазол связывается с атомом железа гематиновой группы и инактивирует 14-α-деметилазу, что приводит к нарушению синтеза эргостерола и накоплению ланостерола и других стеролов. Их включение в мембрану вместо эргостерола значительно нарушает структуру и функцию клеточной мембраны грибов.
Снижение синтеза эргостерола, а также накопление 14α-метилстеролов разрушает плотно упакованные ацильные цепи фосфолипидов мембран грибов. Дестабилизация грибковой мембраны приводит к дисфункции мембранных ферментов, в том числе участвующих в цепи транспорта электронов, и в конечном итоге к гибели клеток.
Применяют при системных микозах: кандидамикозе, криптококкозе, бластомикозе, гистоплазмозе, кокцидиоидомикозе, а также при дерматомикозах. Относительно низкий токсический профиль и высокая степень проникновения в спинномозговую жидкость делают флуконазол препаратом выбора при системном кандидозе и криптококковом менингите. Вследствие осложнений, связанных с интратекальным введением амфотерицина B, флуконазол — препарат первого ряда при кокцидиоидовом менингите. Хотя флуконазол и активен в отношении возбудителей бластомикоза, гистоплазмоза, споротрихоза, он уступает по эффективности в отношении возбудителей этих инфекций итраконазолу. Флуконазол неэффективен при аспергиллезе.
Опыт применения микофлюкана (флуконазола) при лечении фарингомикоза
Проблема диагностики и лечения грибковых заболеваний ЛОР-органов остается актуальной, так как тенденция к снижению удельного веса данной патологии в структуре ЛОР-заболеваний в настоящее время отсутствует. Особенно в последние годы возросла заболеваемость фарингомикозами. Слизистая оболочка глотки, в том числе и миндалин, служит входными воротами для грибковой инфекции. Основными возбудителями микозов слизистой оболочки ротоглотки являются различные виды дрожжеподобных грибов рода Candida. Частота кандидозного фарингита и кандидозного тонзиллита за последние 10 лет резко возросла и составляет 30-45% в структуре инфекционных поражений глотки и миндалин [1, 2]. Рост числа больных фарингомикозами обусловлен существенным увеличением факторов риска их развития, среди которых ведущие позиции занимают ятрогенные иммунодефицитные состояния, возникающие вследствие массивной антибиотикотерапии, длительного использования глюкокортикоидных и иммуносупрессивных препаратов при онкозаболеваниях, болезнях крови, СПИДе, при трансплантации органов, а также в случаях, когда имеет место тяжелая соматическая патология, например сахарный диабет. При этом создаются оптимальные предпосылки для развития фарингомикоза, возбудителями которого являются оппортунистические грибы рода Candida, которые могут сапрофитировать на слизистой оболочке ротоглотки и в окружающей среде и при вышеперечисленных условиях активно размножаются, становятся патогенными.
Проблема выявления и рационального лечения фарингомикозов приобретает важное значение не только вследствие их все более широкого распространения, но также и потому, что грибковые хронические тонзиллиты и фарингиты протекают тяжелее, чем другие воспалительные процессы той же локализации, и могут явиться первичным очагом диссеминированного висцерального микоза, либо стать причиной грибкового сепсиса. Несмотря на создание и внедрение в клиническую практику большого числа местных и ряда системных противогрибковых препаратов, лечение кандидозного фарингита и кандидозного тонзиллита представляет собой достаточно сложную задачу. При этом проблематичным представляется подбор терапии для больных со сформировавшейся резистентностью грибов к различным антимикотическим средствам. Во многом это обусловлено естественной устойчивостью определенных видов грибов рода Candida к используемым в клинической практике противогрибковым препаратам. Большинство из них обладают в основном фунгистатическим действием, что и способствует формированию устойчивости к антимикотикам [4].
Как и другие препараты группы азолов, флуконазол угнетает образование эргостерола, основного компонента клеточной мембраны грибов, действуя на фермент 14a-деметилазу, входящий в систему цитохрома Р450. Нарушение биосинтеза мембраны обусловливает фунгистатический эффект препарата, а в более высоких концентрациях — повреждения мембраны, в ходе перекисного окисления и других процессов приводит к гибели клетки гриба (фунгицидный эффект). В отличие от других азольных препаратов флуконазол обладает высокой специфичностью по отношению к зависимым от цитохрома Р450 ферментам гриба.
Целью настоящей работы явилась оценка эффективности нового препарата из группы азолов микофлюкана в лечении кандидозных заболеваний ротоглотки.
Микофлюкан (флуконазол) — представитель класса триазольных противогрибковых средств — является мощным селективным ингибитором синтеза стеролов в клетке грибов. Для того чтобы ингибиторы эргостеролового синтеза начали действовать, необходимо обеспечить условия для их проникновения внутрь грибковой клетки, накопления в достаточной концентрации, перемещения к микросомам, на которых расположен фермент-мишень, и связь с этим ферментом [3]. Микофлюкан (флуконазол), разработанный (Индия), высоко эффективен при оппортунистических микозах. Высокую эффективность и хорошую переносимость микофлюкана (флуконазола) при приеме внутрь для лечения кандидозного вульвовагинита отметили А. С. Анкирская и соавторы [5], С. Н. Роговская и соавторы [6], В. П. Сметник и соавторы [3]. Для лечения фарингомикоза этот препарат не использовался. Нами были проведены клинические испытания микофлюкана в ходе терапии 44 больных с фарингомикозом, из них 28 человек — с грибковым хроническим фарингитом и 16 — с грибковым хроническим тонзиллитом. В число 28 пациентов с грибковым фарингитом входили 16 женщин и 12 мужчин в возрасте от 17 до 53 лет. Длительность заболевания составляла от 2 мес до 7 лет. Из 16 больных с хроническим грибковым тонзиллитом были обследованы 9 женщин и 7 мужчин в возрасте от 32 до 58 лет. Длительность заболевания — от 3 до 15 лет. Всем больным были проведены общие клинические и микологические исследования. Диагностика заболевания включала анализ результатов следующих исследований:
- Изучение объективной клинической картины заболевания в очаге поражения, т. е. в месте обитания гриба, включая описание всех клинических проявлений, а также вид и характер патологического отделяемого.
- Изучение особенностей гриба в патологическом материале методом микроскопического исследования нативных и окрашенных препаратов.
- Выяснение культуральных особенностей гриба, предусматривающее описание первоначальных колоний грибов, полученных при посевах патологического материала на различные питательные среды.
- Идентификация вида гриба с применением ряда сред и изучение как микроскопической картины гриба, особенностей его развития, так и его биологической активности.
Клиническое течение фарингомикоза у таких больных характеризовалось рядом особенностей. При хроническом грибковом тонзиллите основными жалобами больных являются боли в горле, ощущения инородного тела, покалывание, зуд в горле, жжение. Объективно: гиперемия, отечность дужек (как передней, так и задней) без видимой инфильтрации, что отличает грибковый процесс от бактериального; сами миндалины гиперемированы, лакуны расширены, слизистая оболочка частично эрозирована. Одним из характерных объективных признаков микотического заболевания миндалин является наличие налетов как на миндалинах, так и на дужках; иногда налеты распространяются и на другие отделы ротоглотки. Налеты образуются не только в период обострения, но и при отсутствии обострения хронического тонзиллита. Чаще всего они небольшого размера, точечные или островчатые, расположены около лакун миндалин, они беловатого цвета, творожистого характера, мягкие, легко снимаются. Для грибкового хронического тонзиллита характерны частые обострения (от 2 до 10 раз в год).
Грибковые хронические фарингиты отличаются от микоза миндалин в основном локализацией патологического процесса. Характерным клиническим признаком хронического фарингита грибковой этиологии является неравномерная гиперемия и инфильтрация слизистой оболочки задней стенки ротоглотки. На фоне субатрофии отмечаются увеличение боковых валиков и единичный, округлой формы инфильтративный воспалительный процесс в центре. Наличие небольших налетов также есть признак микотического фарингита. Характер воспаления — хронический, сопровождающийся частыми обострениями.
В результате микологической диагностики были установлены возбудители фарингомикоза у 44 больных. При грибковом фарингите — Candida albicans (22), Candida krusei (2), Candida tropicalis (3), Candida guilliermondi (1). При грибковом хроническом тонзиллите — Candida albicans (10), Candida stellatoidea (3), Candida intermedia (2), Candida pseudotropicalis (1). Всем больным назначали препарат микофлюкан перорально в дозе по 50 мг
1 раз в сутки. Продолжительность лечения при хроническом грибковом фарингите составила 14 дней, при грибковом хроническом тонзиллите — 20 дней.
Контрольное клиническое и микологическое обследование проводилось через 10 дней, через 1 мес и через 2 мес после приема препарата. Результаты лечения представлены в таблице.
Таким образом, в результате лечения 44 больных фарингомикозом микофлюканом излечение, подтвержденное микологическим и клиническим исследованиями, было достигнуто у 29 (65%), улучшение — у 14 (33%), не отмечено эффекта — у 1(2%) больного. При анализе результатов исследования отдельно по нозологическим группам (форма заболевания) удалось установить, что излечение грибкового процесса при кандидозном фарингите было достигнуто у 71% пациентов, а при кандидозном тонзиллите — у 56%. Это вполне объяснимо, поскольку грибковый хронический тонзиллит представляет собой более тяжелое заболевание, чем хронический грибковый фарингит, и терапия его сопряжена с большими трудностями и при применении других антимикотических средств редко бывает достаточно эффективной. Установлена отчетливая зависимость эффективности лечения от длительности заболевания. Во всех случаях, когда терапия была безрезультатной (1) или не было достигнуто полного излечения, длительность грибкового процесса составляла от 7 до 15 лет. Проведенное исследование не позволило выявить взаимосвязи между результативностью лечения и видом гриба — возбудителя заболевания. По-видимому, микофлюкан обладает фунгицидным действием на все виды Candida, которые были выявлены как возбудители фарингомикоза в настоящем исследовании.
Следует отметить хорошую переносимость препарата. При приеме микофлюкана не было зарегистрировано каких-либо побочных реакций и проявлений аллергии.
На основании всего вышеизложенного можно сделать вывод, что в целом положительный эффект от лечения микофлюканом 44 больных фарингомикозом был достигнут у 97% больных.
Нами также проведены сравнительные клинические исследования эффективности другого препарата азольного ряда — дифлюкана (флуконазола) . В настоящее время этот системный препарат широко используется при различных микозах, в основном кандидозной этиологии.
В сравнительных клинических испытаниях дифлюкана (флуконазола) приняли участие 27 больных фарингомикозом (15 женщин и 12 мужчин в возрасте от 17 до 58 лет) с длительностью заболевания от 3 мес до 8 лет. Возбудителями заболевания были Candida albicans (21), Candida stellatoidea (4), Candida krusei (2). У всех больных проводились общие клинические и микологические исследования, аналогичные тем, которые осуществлялись в ходе обследования больных при терапии микофлюканом. Лечение дифлюканом проводили в аналогичных дозах, что и при терапии микофлюканом, т. е. по 50 мг 1 раз в сутки. Продолжительность лечения составила: при хроническом грибковом фарингите — 14 дней, при хроническом грибковом тонзиллите — 20 дней.
В результате терапии 27 больных фарингомикозом препаратом дифлюкан излечение, подтвержденное микологическими и клиническими исследованиями, было достигнуто у 18 больных, улучшение — у 8 и без эффекта — у одного. Таким образом, излечения удалось достичь в 66% случаев, и в целом положительный эффект от лечения препаратом дифлюкан был получен у 96% больных фарингомикозом. Переносимость препарата оценивалась как хорошая. Только у трех больных в процессе лечения отмечались абдоминальные явления в виде тошноты, диспепсии, диареи.
Таким образом, при сравнительном анализе эффективности терапии препаратами класса азолов: микофлюканом и дифлюканом — были получены аналогичные результаты. Переносимость микофлюкана оказалась более высокой, так как ни в одном случае не было отмечено побочных реакций на фоне его приема, что в значительной степени повышает приверженность пациентов к лечению этим препаратом.
Таким образом, высокая эффективность препарата микофлюкан (флуконазол) при лечении больных фарингомикозом (положительный эффект 97%), его хорошая переносимость и удобство в применении (1 раз в сутки) позволяют считать это лекарственное средство наиболее перспективным при терапии хронического тонзиллита и хронического фарингита кандидозной этиологии.
Литература
- Кунельская В. Я. Микозы в оториноларингологии. — М.: Медицина, 1989. — 320 с.
- Старосветский Б. М. Хронический фарингит грибковой этиологии: Дис. … канд. мед. наук. — М., 1990.
- Сметник В. П., Марченко Л. А., Чернуха Г. Е. Опыт применения Микофлюкана (флуконазола) для лечения кандидозного вульвовагинита // Лечащий Врач. — 2004. — № 2. — С. 2 — 3.
- Маликов В. Е., Жарикова Н. Е., Романовская Т. А., Рассказов Д. Н. Этиология вагинального кандидоза и проблема устойчивости к антимикотикам // Контрацепция и здоровье женщин. — 2002. — № 1. — С. 9 — 16.
- Анкирская А. С., Муравьева В. В., Демидова Е. М., Карпова О. Ю., Зайдиева Я. З., Фурсова С. А. Дифлюкан 150: опыт лечения и профилактика вагинального кандидоза // Вестник дерматологии и венерологии. — 1998. — № 3. — С. 65 — 67.
- Роговская С. Н., Прилепская В. Н., Байрамова Г. Р. Опыт применения дифлюкана при лечении генитального кандидоза // Вестник дерматологии и венерологии. — 1997. — № 1. — С. 100 — 101.
В. Я. Кунельская, доктор медицинских наук, профессор ГКБ № 31, Москва
Фармакокинетика
После приема внутрь флуконазол хорошо всасывается, прием пищи не влияет на скорость всасывания флуконазол а, его биодоступность — 90%.
Время максимальной концентрации после приема внутрь, натощак 150 мг препарата 0,5-1,5 ч и составляет 90% от концентрации в плазме при внутривенном введении в дозе 2,5-3,5 мг/л. Период полувыведения флуконазола составляет 30 ч. Связь с белками плазмы 11-12%. Концентрация в плазме находится в прямой зависимости от дозы. 90% уровень равновесной концентрации достигается к 4-5 дню лечения препаратом (при приеме 1 раз/сут).
Введение «ударной» дозы (в первый день), в 2 раза превышающей обычную суточную дозу, позволяет достичь уровня концентрации, соответствующий 90% равновесной концентрации, ко второму дню.
Флуконазол хорошо проникает во все биологические жидкости организма. Концентрация активного вещества в грудном молоке, суставной жидкости, слюне, мокроте и перитонеальной жидкости аналогична таковой в плазме крови. Постоянные значения в вагинальном секрете достигаются через 8 ч после приема внутрь и удерживаются на этом уровне не менее 24 ч.
Фармакокинетика флуконазола существенно зависит от функционального состояния почек, при этом существует обратная зависимость между периодом полувыведения и клиренсом креатинина. После гемодиализа в течение 3 ч концентрация флуконазола в плазме снижается на 50%.
Флуконазол Канон (50мг, 150мг)
Однократный или многократный прием флуконазола в дозе 50 мг не влияет на метаболизм феназона (Антипирина) при их одновременном приеме.
Одновременное применение флуконазола со следующими препаратами противопоказано:
Цизаприд: при одновременном применении флуконазола с цизапридом возможны нежелательные реакции со стороны сердца, включая аритмию желудочковую тахисистолическую типа «пируэт» (torsade de pointes). Применение флуконазола в дозе 200 мг 1 раз в сутки и цизаприда в дозе 20 мг 4 раза в сутки приводит к выраженному увеличению плазменных концентраций цизаприда и увеличение интервала QT на ЭКГ. Одновременный прием цизаприда и флуконазола противопоказан.
Терфенадин: при одновременном применении азольных противогрибковых средств и терфенадина возможно возникновение серьезных аритмий в результате увеличения интервала QT. При приеме флуконазола в дозе 200 мг/сутки увеличения интервала QT не установлено, однако применение флуконазола в дозах
400 мг/сутки и выше вызывает значительное увеличение концентрации тефенадина в плазме крови. Одновременный прием флуконазола в дозе 400 мг/сутки и более с терфенадином противопоказан (см. раздел «Противопоказания»). Лечение флуконазолом в дозах менее 400 мг/сутки в сочетании с терфенадином следует проводить под тщательным контролем.
Астемизол: одновременное применение флуконазола с астемизолом или другими препаратами, метаболизм которых осуществляется системой цитохрома P450, может сопровождаться повышением сывороточных концентраций этих средств. Повышенные концентрации астемизола в плазме крови могут приводить к удлинению интервала QT и, в некоторых случаях, к развитию аритмии желудочковой тахисистолической типа «пируэт» (torsade de pointes). Одновременное применение астемизола и флуконазола противопоказано.
Пимозид: соответствующих исследований in vitro или in vivo не проводилось, однако, одновременное применение флуконазола и пимозида может приводить к угнетению метаболизма пимозида. В свою очередь повышение плазменных концентраций пимозида может приводить к удлинению интервала QT и, в некоторых случаях, к развитию аритмии желудочковой тахисистолической типа «пируэт» (torsade de pointes). Одновременное применение пимозида и флуконазола противопоказано.
Хинидин: несмотря на то, что не проводилось исследований in vitro или in vivo, одновременное применение флуконазола и хинидина может также приводить к угнетению метаболизма хинидина. Применение хинидина связано с удлинением интервала QT и, в некоторых случаях, может приводить к развитию аритмии желудочковой тахисистолической типа «пируэт» (torsade de pointes). Одновременное применение флуконазола и хинидина противопоказано.
Эритромицин: одновременное применение флуконазола и эритромицина потенциально приводит к повышенному риску развития кардиотоксичности (удлинение интервала QT, torsade de pointes) и, вследствие этого, внезапной сердечной смерти. Одновременное применение флуконазола и эритромицина противопоказано.
Амиодарон: совместное применение флуконазола и амиодарона может привести к ингибированию метаболизма амиодарона. Применение амиодарона ассоциировалось с удлинением интервала QT. Одновременное применение флуконазола и амиодарона противопоказано (см. раздел «Противопоказания»).
Следует соблюдать осторожность и, возможно, корректировать дозы при одновременном употреблении флуконазола и следующих препаратов
Препараты, влияющие на флуконазол:
Гидрохлоротиазид: многократное применение гидрохлоротиазида одновременно с флуконазолом приводит к увеличению концентрации флуконазола в плазме крови на 40 %. Эффект такой степени выраженности не требует изменения режима дозирования флуконазола у пациентов, получающих одновременно и диуретики, однако врачу следует это учитывать.
Рифампицин: комбинация с рифампицином приводит к снижению площади под кривой «концентрация-время» (AUC) на 25 % и укорочению периода полувыведения флуконазола из плазмы на 20 %. Поэтому больным, получающим одновременно рифампицин, дозу флуконазола целесообразно увеличить.
Препараты, на которые влияет флуконазол
Флуконазол является мощным ингибитором изофермента CYP2C9 и CYP2C19 цитохрома P450 и умеренным ингибитором изофермента CYP3A4. Кроме того, помимо перечисленных далее эффектов, существует риск повышения в плазме крови концентрации и других лекарственных средств, метаболизируемых изоферментами CYP2C9, CYP2C19 и CYP3A4 при одновременном приеме с флуконазолом. В связи с этим при одновременном применении перечисленных препаратов и флуконазола следует соблюдать осторожность, при необходимости таких комбинаций, пациенты должны находиться под тщательным медицинским наблюдением. Следует учитывать, что ингибирующий эффект флуконазола сохраняется в течение 4-5 дней после отмены препарата в связи с длительным периодом полувыведения.
Тофацитиниб: экспозиция тофацитиниба увеличивается при его совместном применении с препаратами, которые являются одновременно умеренными ингибиторами изофермента CYP3A4 и мощными ингибиторами изофермента CYP2C19 (каким является флуконазол). Возможно, может понадобиться коррекция дозы тофацитиниба.
Алфентанил: отмечается уменьшение клиренса и объема распределения, увеличение периода полувыведения алфентанила. Возможно, это связано с ингибированием изофермента CYP3A4 флуконазолом. Может потребоваться коррекция дозы алфентанила.
Амитриптилин, нортриптилин: увеличение эффекта. Концентрацию 5-нортриптилина и/или S-амитриптилина можно измерить в начале комбинированной терапии с флуконазолом и через неделю после начала лечения. При необходимости следует корректировать дозу амитриптилина/нортриптилина.
Амфотерицин В: в исследованиях на мышах (в том числе с иммуносупрессией) были отмечены следующие результаты: небольшой аддитивный противогрибковый эффект при системной инфекции, вызванной C. albicans, отсутствие взаимодействия при внутричерепной инфекции, вызванной Criptococcus neoformans, и антагонизм при системной инфекции, вызванной A. fumigatus. Клиническое значение данных результатов не известно.
Антикоагулянты: как и другие противогрибковые средства (производные азола), флуконазол, при одновременном применении с варфарином, повышает протромбиновое время (на 12 %), в связи с чем, возможно развитие кровотечений (гематомы, кровотечения из носа и желудочно-кишечного тракта, гематурия, мелена). У пациентов, получающих кумариновые антикоагулянты и флуконазол, необходимо постоянно контролировать протромбиновое время в период терапии и в течение 8 дней после одновременного применения. Также следует оценить целесообразность коррекции дозы варфарина.
Азитромицин: при одновременном применении внутрь флуконазола в однократной дозе 800 мг с азитромицином в однократной дозе 1200 мг выраженного фармакокинетического взаимодействия не установлено.
Бензодиазепины (короткого действия): после приема внутрь мидазолама флуконазол существенно увеличивает его концентрацию и психомоторные эффекты, причем это влияние более выражено после приема флуконазола внутрь, чем при его внутривенном введении. При необходимости сопутствующей терапии бензодиазепинами пациентов, принимающих флуконазол, следует наблюдать с целью оценки целесообразности соответствующего снижения дозы бензодиазепина.
При одновременном приеме однократной дозы триазолама флуконазол увеличивает AUC триазолама приблизительно на 50%, Cmax — на 25-50 % и период полувыведения — на 25-50 %, благодаря угнетению метаболизма триазолама. Может понадобиться коррекция дозы триазолама.
Карбамазепин: флуконазол угнетает метаболизм карбамазепина и повышает сывороточную концентрацию карбамазепина на 30 %. Необходимо учитывать риск развития токсичности карбамазепина. Следует оценить необходимость коррекции дозы карбамазепина в зависимости от концентрации/эффекта.
Блокаторы кальциевых каналов: некоторые антагонисты кальциевых каналов (нифедипин, амлодипин, верапамил и фелодипин) метаболизируются изоферментом CYP3A4. Флуконазол может увеличивать системное действие антагонистов кальциевых каналов. Рекомендуется контролировать развитие побочных эффектов.
Циклоспорин: у пациентов с пересаженной почкой прием флуконазола в дозе
200 мг/сутки приводит к медленному повышению концентрации циклоспорина в плазме. При многократном применении флуконазола в дозе 100 мг/сутки изменения концентрации циклоспорина у реципиентов костного мозга не наблюдалось. Рекомендуется контролировать концентрацию циклоспорина в крови у пациентов, получающих флуконазол.
Циклофосфамид: при одновременном применении циклофосфамида и флуконазола отмечается увеличение сывороточных концентраций билирубина и креатинина. Данная комбинация допустима с учетом риска увеличения концентраций билирубина и креатинина.
Фентанил: имеется сообщение о смертельном исходе, возможно, связанном с одновременным применением флуконазола и фентанила. Флуконазол значительно удлиняет время выведения фентанила. Побочные эффекты, возможно, связаны с интоксикацией фентанилом. Следует учитывать, что повышение концентрации фентанила может привести к угнетению дыхания.
Галофантрин: в связи с ингибированием изофермента CYP3A4 флуконазол может увеличивать концентрацию галофантрина в плазме крови. При одновременном применении с флуконазолом и другими противогрибковыми препаратами азолового ряда возможно развитие аритмии желудочковой тахисистолической типа «пируэт» (torsade de pointes). Совместное их применение не рекомендуется.
Ингибиторы ГМГ-КоА-редуктазы: при одновременном применении флуконазола с ингибиторами ГМГ-КоА-редуктазы, которые метаболизируются изоферментом CYP3A4 (например, аторвастатин, симвастатин) или изоферментом CYP2D6 (флувастатин), увеличивается риск развития миопатии и рабдомиолиза. В случае необходимости одновременной терапии данными препаратами следует наблюдать пациентов с целью выявления симптомов миопатии и рабдомиолиза. Необходимо контролировать концентрацию креатинкиназы. В случае значительного увеличения концентрации данного фермента или если диагностируется, или имеется подозрение на развитие миопатии или рабдомиолиза, терапию ингибиторами ГМГ-КоА-редуктазы следует прекратить.
Лозартан: флуконазол угнетает метаболизм лозартана до его активного метаболита (Е-3174), который отвечает за большую часть эффектов, связанных с антагонизмом ангиотензин-II рецепторов. Необходим регулярный контроль артериального давления.
Метадон: флуконазол может увеличивать плазменную концентрацию метадона. Может понадобиться коррекция дозы метадона.
Нестероидные противовоспалительные препараты (НПВП): Cmax и AUC флубипрофена увеличиваются на 23 % и 81 % соответственно. При одновременном применении флуконазола и рацемического ибупрофена
(400 мг) Cmax и AUC фармакологически активного изомера [S-(+)-ибупрофен] повышались на 15 % и 82 % соответственно. При одновременном применении флуконазола в дозе 200 мг/сутки и целекоксиба в дозе 200 мг Cmax и AUC целекоксиба увеличиваются на 68 % и 134 % соответственно. В данной комбинации возможно снижение дозы целекоксиба вдвое.
Флуконазол может увеличивать системную экспозицию других НПВП, метаболизируемых изоферментом CYP2C9 (например, напроксен, лорноксикам, мелоксикам, диклофенак), однако целенаправленных исследований не проводилось. Может потребоваться коррекция дозы НПВП.
При одновременном применении флуконазола и НПВП пациенты должны находиться под тщательным медицинским наблюдением с целью выявления и контроля нежелательных явлений и проявлений токсичности, связанных с НПВП.
Пероральные контрацептивы: при одновременном применении комбинированного перорального контрацептива с флуконазолом в дозе 50 мг существенного влияния на уровень гормонов не установлено. При ежедневном употреблении 200 мг флуконазола AUC этинилэстрадиола и левоноргестрела увеличиваются на 40 % и 24 % соответственно, при приеме 300 мг флуконазола один раз в неделю AUC этинилэстрадиола и нортэтиндрона возрастают на 24 % и 13 % соответственно. Таким образом, многократное применение флуконазола в указанных дозах с малой вероятностью оказывает влияние на эффективность комбинированного перорального контрацептива.
Фенитоин: одновременное применение флуконазола и фенитоина может привести к возрастанию концентрации фенитоина в плазме до клинически значимой степени. Поэтому при необходимости совместного применения этих препаратов необходимо мониторировать концентрации фенитоина с коррекцией его дозы с целью поддержания концентрации препарата в пределах терапевтического интервала.
Преднизон: имеется сообщение о развитии острой недостаточности коры надпочечников у пациента после трансплантации печени на фоне отмены флуконазола после трехмесячного курса терапии. Предположительно, прекращение терапии флуконазолом вызвало повышение активности изофермента CYP3A4, что привело к увеличенному метаболизму преднизона. Пациенты, получающие комбинированную терапию преднизоном и флуконазолом, должны находиться под тщательным медицинским наблюдением при отмене приема флуконазола с целью оценки состояния коры надпочечников.
Рифабутин: одновременное применение флуконазола и рифабутина может сопровождаться повышением сывороточной концентрации последнего до 80%. При одновременном применении флуконазола и рифамбутина описаны случаи увеита. Необходимо тщательно наблюдать пациентов, одновременно получающих рифабутин и флуконазол.
Саквинавир: при совместном применении, AUC саквинавира повышается приблизительно на 50 %, Cmax — на 55 %, клиренс уменьшается на 50 %, в связи с ингибированием изофермента CYP3A4 и ингибированием Р-гликопротеина. Может понадобиться коррекция дозы саквинавира.
Сиролимус: при одновременном применении наблюдается увеличение концентрации сиролимуса в плазме крови, связанное, вероятно, с ингибированием изофермента CYP3A4 и Р-гликопротеина. Данная комбинация может применяться с соответствующей коррекцией дозы сиролимуса в зависимости от эффекта/концентрации.
Препараты сульфонилмочевины: флуконазол увеличивает период полувыведения из плазмы пероральных гипогликемических средств — производных сульфонилмочевины (хлорпропамид, глибенкламид, глипизид, толбутамид). Совместное применение флуконазола и пероральных гипогликемических средств у пациентов с сахарным диабетом допускается, однако врач должен иметь в виду возможность развития гипогликемии. Необходим регулярный контроль уровня глюкозы в крови и, при необходимости, коррекция дозы препаратов сульфонилмочевины.
Такролимус: флуконазол при одновременном применении повышает концентрацию такролимуса (внутрь) в плазме крови в 5 раз за счет ингибирования метаболизма такролимуса, происходящего в кишечнике с участием изофермента CYP3A4. В связи с этим, возрастает риск нефротоксического действия. Пациентов, принимающих такролимус внутрь, следует тщательно наблюдать. Дозу такролимуса следует корректировать в зависимости от степени повышения его концентрации в крови. При применении такролимуса внутривенно значительных изменений в фармакокинетике препарата не наблюдается.
Теофиллин: при одновременном применении с флуконазолом в дозе 200 мг в течение 14 дней средняя скорость плазменного клиренса теофиллина снижается на 18 %. Больные, которые получают высокие дозы теофиллина или у которых имеется вероятность развития теофиллиновой интоксикации, должны находиться под наблюдением с целью раннего выявления симптомов передозировки теофиллина. При необходимости терапия должна быть скорректирована соответствующим образом.
Алкалоид барвинка: флуконазол может увеличивать концентрацию алкалоидов барвинка (винкристина и винбластина) в плазме крови и способствовать к проявлению нейротоксичности. Это может быть связано с угнетением изофермента CYP3A4, однако, целенаправленные исследования не проводились.
Витамин А: имеется сообщение об одном случае развития нежелательных реакций со стороны центральной нервной системы (ЦНС) в виде псевдоопухоли мозга при одновременном применении флуконазола с полностью трансретиноевой кислотой, которые исчезли после отмены флуконазола. Применение данной комбинации возможно, но следует учитывать возможность развития нежелательных реакций со стороны ЦНС.
Зидовудин: у пациентов, получающих комбинацию флуконазола и зидовудина, наблюдается увеличение Cmax и AUC зидовудина на 84 % и 74 % соответственно, которое вызвано снижением превращения последнего в его главный метаболит. До и после терапии флуконазолом в дозе 200 мг/сутки в течение 15 дней больным СПИДом и ARC (комплекс, связанный со СПИДом) установлено значительное увеличение AUC зидовудина (20 %). При совместном применении следует ожидать увеличения побочных эффектов зидовудина.
Невирапин: одновременное применение флуконазола и невирапина приводит к увеличению воздействия невирапина примерно на 100%. В случае одновременного применения этих препаратов, сопровождающегося риском повышенного воздействия невирапина, необходимо соблюдать осторожность и тщательно наблюдать пациентов. Клинически значимого влияния невирапина на флуконазол не отмечалось.
Вориконазол (ингибитор изоферментов CYP2C9, CYP2C19 и CYP3A4): одновременное применение флуконазола и вориконазола (по 400 мг 2 раза в сутки в первый день, затем по 200 мг два раза в сутки в течение 2,5 дней) и флуконазола (по 400 мг в первый день, затем по 200 мг два раза в сутки в течение 4 дней) приводит к увеличению концентрации и AUC вориконазола на 57 % и 79 % соответственно. Было показано, что данный эффект сохраняется при уменьшении дозы и/или уменьшении кратности приема любого из препаратов. Одновременное применение вориконазола и флуконазола не рекомендуется.
Ивакафтор: при одновременном применении с ивакафтором, стимулятором муковисцидозного регулятора трансмембранной проводимости (CFTR), наблюдалось увеличение экспозиции ивакафтора в 3 раза и экспозиции гидроксиметил-ивакафтора (М1) в 1,9 раза. Пациентам, одновременно принимающим умеренные ингибиторы CYP3A, такие как флуконазол и эритромицин, рекомендуется снижение дозы ивакафтора до 150 мг один раз в сутки.
Исследования взаимодействия флуконазола при его одновременном приеме с пищей, циметидином, антацидами, а также после тотального облучения тела для подготовки к пересадке костного мозга показали, что эти факторы не оказывают клинически значимого влияния на всасывание флуконазола.
Перечисленные взаимодействия установлены при многократном применении флуконазола; взаимодействия с лекарственными средствами в результате однократного приема флуконазола не известны. Врачам следует учитывать, что взаимодействие с другими лекарственными средствами специально не изучалось, но оно возможно.
Показания к применению
Показаниями к применению капсул Флуконазол являются:
- Криптококковая инфекция, включая специфическое поражение оболочек головного мозга (криптококковый менингит) у пациентов на фоне иммунодефицита или с нормальным состоянием функциональной активности иммунитета.
- Тяжелая форма кандидоза с генерализацией инфекционного процесса и поражением значительного объема тканей (слизистые оболочки различных органов, кожа, брюшина, эндокард, глаза, дыхательные и мочевые пути). В большинстве случаев инфекция развивается на фоне выраженного снижения функциональной активности иммунной системы при злокачественных новообразованиях, лечении цитостатиками, иммуносупрессорами, а также у пациентов, находящихся длительное время в отделении интенсивной терапии.
- Локализованный кандидоз, развивающийся на слизистых оболочках полости рта и верхних отделов пищеварительного тракта, на структурах урогенитального тракта – препарат в лекарственной форме для системного применения используется в случае недостаточной эффективности мази или крема для местного применения.
- Дерматомикозы, которые локализуются на коже стоп, туловища, паховой области.
- Отрубевидный (разноцветный) лишай.
- Грибковое поражение ногтевых пластинок (онихомикоз).
- Глубокие эндемические микозы, которые могут включать паракокцидиомикоз, кокцидиомикоз, гистоплазмоз у пациентов с нормальной функциональной активностью иммунитета.
Препарат также применяется для профилактики развития грибковой инфекции у пациентов с нормальным или нарушенным иммунитетом.
Этапы развития кандидозного стоматита
Лечение кандидозного стоматита зависит от степени его прогрессирования. Всю болезнь по симптомам можно разделить на несколько этапов в зависимости от того, насколько поздно она выявлена:
- Этап первый. Самые легкие симптомы кандидоза полости рта — появление красных язвочек на слизистой: щеках, губах, а также на деснах, языке и миндалинах. На этой стадии лечение кандидозного стоматита затруднено из-за того, что заболевание еще мало заметно и может не вызывать серьезного дискомфорта, из-за чего пациент не обращается к врачу. Первый этап может продолжаться достаточно долго и не развиваться в последующие.
- Этап второй. На местах язвочек возникает белый творожистый налет, который можно удалить. При соскабливании на месте язвочек образуются красные и довольно болезненные ранки. На этом этапе может повышаться температура, однако незначительно и довольно редко.
- Этап третий. Белый творожистый налет становится очень трудно соскоблить, ранки кровоточат и сильно болят. Этот период опасен тем, что в кровоточащие ранки могут попасть микроорганизмы, которые вызовут уже бактериальный стоматит, течение которого проходит тяжелее и сопровождается очень высокой температурой.
- Этап четвертый. Тяжелая форма кандидозного стоматита, требующая немедленных мер. Могут поражаться верхние дыхательные пути, поэтому как именно лечить кандидозный стоматит может определить только специалист. На этой стадии болезнь очень опасна для детей.
Кроме того, важно знать также и о том, что кандидозный стоматит — это заразное заболевание, которое передается через поцелуи и даже через общую посуду. Рекомендуем пройти полное лечение кандидозного стоматита и не допускать во время болезни подобных контактов с другими людьми.
Способ применения и дозировка
Капсулы Флуконазол предназначены для приема внутрь. Их не разжевывают и запивают достаточным количеством жидкости. Дозировка и режим применения препарата зависят от медицинских показаний:
- Криптококковый менингит у взрослых и детей старше 15-ти лет – в первый день препарат назначается в дозировке 400 мг в сутки, затем переходят на поддерживающую дозу 200 мг в день.
- Профилактика обострения криптококкового менингита у пациентов с выраженным иммунодефицитом, в частности на фоне СПИДа – после завершения курса первичной терапии, направленной на максимальное уничтожение возбудителя заболевания препарат назначается в суточной дозировке 200 мг.
- Генерализованный кандидоз – в первые дни назначается 400 мг в день, затем переходят на 200 мг в день. В случае отсутствия достаточного терапевтического эффекта снова переходят на дозу 400 мг.
- Кандидоз, локализующийся на слизистой оболочке полости рта, пищевода – 150 мг 1 раз в день от 14 до 28 дней (в зависимости от скорости достижения терапевтического результата).
- Вагинальный кандидоз у женщин (молочница) – 150 мг однократно, для профилактики обострения через 1 месяц прием препарата повторяется. Иногда при недостаточной эффективности и хроническом течения данной формы кандидоза врач устанавливает дозировку и режим применения, включая длительность курса терапии, индивидуально.
- Профилактика кандидоза различной локализации – дозировка устанавливается врачом индивидуально, она может варьировать от 50 до 400 мг в день.
- Отрубевидный лишай – 300 мг в день 1 раз в неделю в течение 3-х недель, данная схема при необходимости может корригироваться лечащим врачом.
- Дерматомикозы, включая поражение кожи стоп – 150 мг 1 раз в неделю 3-4 недели.
- Онихомикоз – 150 мг 1 раз в неделю, курс лечения продолжается до полного замещения ногтевой пластинки, при необходимости он может повторяться.
- Глубокие эндемические микозы – дозировка препарата варьирует от 200 до 400 мг в день, длительность курса терапии может достигать 24 месяцев.
Режим применения капсул Флуконазол у детей имеет определенные сходства со взрослыми. Важным условием является избегание превышения дозы 400 мг в сутки. В большинстве случаев режим применения, дозировка и длительность курса терапии устанавливаются врачом индивидуально.
Флуконазол в терапии кандидоза
В
последние годы существенно повысилась распространенность грибковых заболеваний, что связано с широким и не всегда рациональным применением антибиотиков, цитостатиков, кортикостероидных гормонов, повышением частоты внутрибольничных инфекций, развитием иммунодефицитных состояний.
Наиболее часто в клинической практике встречается кандидоз, вызываемый дрожжеподобным грибком Candida albicans
. Развитию кандидоза способствуют как местные, так и системные факторы. Например, при кандидозе кожи большое значение имеет наличие мацерации, опрелости, паронихий. Наиболее часто кандидоз встречается у больных сахарным диабетом, ВИЧ-инфекцией, гемобластозами, а также при длительном и неконтролируемом приеме антибиотиков и кортикостероидных гормонов.
Клинические проявления
кандидоза характеризуются поражением слизистых оболочек полости рта (стоматит), пищевода (эзофагит), урогенитального тракта, кожи и ногтей. К наиболее тяжелым проявлениям приводит гематогенная диссеминация (эндокардиты, менингиты, артриты, остеомиелиты, абсцесс головного мозга).
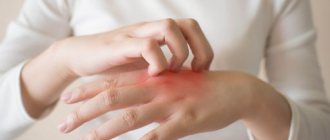
Кожные поражения при кандидозе характеризуются появлением пузырьков, пустул, которые быстро вскрываются и на их месте образуется эрозия. Очаги темно-красного цвета, блестящие, с влажной поверхностью, четкими границами и полоской отслаивающегося рогового слоя эпидермиса. У детей процесс может распространиться на кожу бедер, ягодиц, живота. Часто наблюдается появление межпальцевой кандидозной эрозии, чаще между III и IV IV и V пальцами кистей рук, реже стоп. Из субъективных ощущений отмечаются зуд, жжение, иногда болезненность в области поражения.
Кандидоз слизистой полости рта характеризуется поражением слизистой щек, языка, десен, углов рта. Процесс начинается с покраснения слизистой, затем появляются налеты белого цвета, сливающиеся с образованием крупных пленок. Вначале пленки легко отделяются, затем становятся плотными. В углах рта образуются трещины с выраженной мацерацией, отмечается жжение и болезненность при приеме пищи.
Кандидоз ногтевых валиков и ногтей начинается с покраснения и припухлости валика у основания ногтя, который набухает и при надавливании выделяется гной или сукровица. При внедрении грибковой инфекции в ногтевую пластинку она становится желтоватой, тусклой.
Урогенитальный кандидоз может протекать в острой или хронической форме. Острая форма характеризуется покраснением слизистой, наличием пузырьков, точечных эрозий и наличием творожистых или хлопьевидных, сливкообразных выделений. Пораженная слизистая имеет склонность к кровоточивости и появлению трещин в области преддверия влагалища и промежности. Зуд характерен для кандидоза вульвы, больших и малых половых губ, усиливается во время менструации, полового контакта и при длительной ходьбе. Для хронического урогенитального кандидоза характерны инфильтрация и трещины в области клитора, ануса, промежности и паховых складок. Кандидоз органов мочевыделения протекает в виде уретрита, цистита, пиелонефрита. Кандидозный цистит характеризуется частым мочеиспусканием, болями в надлобковой области. При уретрите появляются слизисто-гнойные выделения белого или желтого цвета, преимущественно в утреннее время. Зуд и жжение усиливаются при мочеиспускании.
Кандидозный баланопостит проявляется покраснением, отечностью головки полового члена, зудом и жжением при мочеиспускании. На соприкасающихся поверхностях головки и крайней плоти образуются пленки желтоватого цвета и рыхлая творожистая масса.
При кандидозе пищеварительного тракта развивается поражение пищевода, желудка, кишечника и желчного пузыря, что связано с распространением инфекции из полости рта и глотки. Больные жалуются на тошноту, отрыжку, рвоту, жидкий стул с примесью слизи, боли в животе. Слизистая оболочка гиперемирована, эрозирована, покрыта множественными налетами белого или желтого цвета.
Кандидозное поражение центральной нервной системы протекает по типу менингита, развивается в результате гематогенной диссеминации инфекции. Специфические клинические проявления отсутствуют, грибковая инфекция часто подтверждается только на аутопсии.
Гематогенная диссеминация грибковой инфекции C. albicans
сопровождается лихорадкой, токсическими и очаговыми проявлениями (абсцесс сетчатки, кандидоз эндокарда, артриты, менингит, пневмония).
Кандидозный сепсис развивается при поражении слизистой оболочки ротовой полости и пищевода у детей раннего возраста и у больных сахарным диабетом, ВИЧ-инфекцией. В клинической картине преобладают симптомы интоксикации, резкие подъемы и спады температуры, снижение артериального давления.
Диагностика кандидоза
основана на клинических проявлениях (зуд, жжение, налеты, отек слизистых, гиперемия и другие), микробиологических тестах (культивирование
in vitro
, гистология и выявление специфических антигенов в реакции иммунофлюоресценции с моноклональными антителами против
C. albicans
, выявление специфических антител методом иммуноферментного анализа).
Для лечения кандидоза
применяют антимикотические препараты системного действия (полиеновые антимикотики, триазольные производные, пиримидиновые производные и аллиламины). Среди триазольных производных ведущее место занимает
флуконазол (Микосист)
, являющийся селективным ингибитором синтеза стеролов в клетке грибка.
Флуконазол высокоактивен в отношении C. albicans
: лишь около 3-5% штаммов
C. albicans
резистентны к флуконазолу или имеют промежуточную чувствительность.
Candida krusei
и отдельные штаммы
Candida glabrata
резистентны к флуконазолу.
После перорального приема флуконазола более 90% препарата попадает в системный кровоток. Он отлично проникает в слюну, мокроту, мочу и другие тканевые жидкости. Выводится флуконазол преимущественно с мочой в неизмененном виде. Период полувыведения при нормальной функции почек – 27-34 ч. Микосист (флуконазол) выпускается в двух формах – для внутривенного и для перорального введения, пероральная форма обладает очень хорошей биодоступностью.
Флуконазол является препаратом выбора при кандидозной инфекции мочевыводящих путей, эзофагите, перитоните, раневой инфекции, используется в лечении фебрильных нейтропений. При урогенитальном кандидозе флуконазол назначают в дозе от 50 до 200 мг в сутки в течение 7-28 дней. При кандидозном эзофагите рекомендуется доза 400 мг с последующим снижением до 200 мг.
Флуконазол считается средством выбора в системной терапии кандидоза полости рта. При орофарингеальном кандидозе флуконазол взрослым назначают в дозе 100 мг один раз в сутки в течение 7-14 дней. При атрофическом кандидозе полости рта предпочтительно назначать флуконазол в дозе 50 мг в сутки в течение 14 дней. При развивающейся устойчивости C. albicans
дозу флуконазола повышают до 400–800 мг/сут. При частых рецидивах возможно назначение пульс–терапии флуконазолом (150 мг 1 раз в неделю). Интермиттирующие схемы позволяют предотвратить развитие устойчивости.
При кандидозе кожи эффективная доза флуконазола колеблется от 50 до 100 мг в сутки в течение 14-28 дней. При кандидозе кожи стоп мы рекомендуем дозу 150 мг в сутки в течение 14-28 дней.
Выбор лечения кандидной паронихии зависит от стадии процесса, выраженности воспаления, наличия кандидоза кожи или слизистых оболочек, онихомикоза. Флуконазол назначают при сопутствующем онихомикозе, сочетании паронихии с кандидозом кожи или слизистых оболочек. В этих случаях только местная терапия не гарантирует излечения и элиминации возбудителя. Флуконазол назначают по 150 мг 1 раз в неделю в течение 2–6 нед. Системную терапию можно сочетать с лечением местными антисептиками или противогрибковыми средствами.
Для профилактики кандидоза при проведении антибиотикотерапии доза флуконазола составляет от 50 до 300 мг в сутки однократно, в зависимости от риска развития грибковой инфекции.
У детей суточная доза составляет 3 мг/кг веса в сутки. В первый день целесообразно назначить ударную дозу 6 мг/кг в сутки. Длительность терапии у детей составляет от 1 до 14 дней, в зависимости от тяжести кандидозной инфекции.
Флуконазол хорошо переносится, побочные реакции встречаются в основном со стороны желудочно-кишечного тракта (боль в животе, тошнота, метеоризм), реже наблюдается головная боль, кожные высыпания.
Противопоказания к применению
Медицинскими противопоказаниями для приема капсул Флуконазол служат патологические и физиологические процессы в организме пациента, к которым относятся:
- Одновременный прием препарата терфинадина, астемизола, а также других лекарственных средств, которые приводят к удлинению интервала QT на электрокардиограмме (особенно в случае применения капсул Флуконазол в суточной дозировке, превышающей 400 мг).
- Детский возраст до 4-х лет.
- Индивидуальная непереносимость основного действующего компонента или дополнительных веществ данного медикаментозного средства.
С осторожностью лекарственное средство используется при сопутствующей печеночной или почечной недостаточности, появлении сыпи на коже у пациентов с генерализованными системными грибковыми инфекциями, одновременное применение препарата в суточной дозировке менее 400 мг с терфенадином, хроническом алкоголизме, в случае применения препаратов, которые обладают гепатотоксическим действием, а также у пациентов с высоким риском развития аритмии (нарушение ритма и частоты сокращений сердца) на фоне органической патологии сердца, нарушений электролитного баланса в организме. Также с осторожностью препарат используется у беременных женщин. Перед назначением капсул Флуконазол врач убеждается в отсутствии противопоказаний у пациента.
Побочные действия
Во время применения препарата Флуконазол возможны побочные действия
- Со стороны иммунной системы: гиперчувствительность (перекрестная со всеми азолами), другие анафилактические, анафилактоидные и аллергические реакции (в том числе синдром Стивенса-Джонсона, токсический эпидермальный некролиз, крапивница).
- Со стороны нервной системы: головная боль, головокружение, периферическая невропатия, парестезии, чрезмерная утомляемость, редко — судороги.
- Со стороны пищеварительной системы: снижение аппетита, сухость слизистой оболочки полости рта, изменения вкуса, боль в животе, рвота, тошнота, диарея, метеоризм, редко — нарушение функции печени (желтуха, гепатит, гепатонекроз, гипербилирубинемия, повышение активности аланинаминотрансферазы, аспартатаминотрансферазы, повышение активности щелочной фосфатазы, гепатоцеллюлярный некроз), в том числе тяжелое.
- Со стороны органов кроветворения: редко — лейкопения, тромбоцитопения (кровотечения, петехии), нейтропения, агранулоцитоз.
- Со стороны сердечно-сосудистой системы: увеличение продолжительности интервала QT, мерцание/трепетание желудочков, пируэтная тахикардия (torsade de pointes).
- Со стороны обмена веществ: гиперхолестеринемия, гипертриглицеридемия, гипокалиемия, гипергликемия.
- Со стороны опорно-двигательного аппарата: миалгия.
- Прочие: слабость, астения, периферические отеки, нейтропения, кожный зуд, отек легких, лихорадка, повышенная потливость, вертиго.
Клинические исследования
Многократно проведенные клинические исследования доказали, что двухкомпонентный ополаскиватель для полости рта АСЕПТА АКТИВ более эффективно борется с причинами воспаления и кровоточивости по сравнению с однокомпонентными ополаскивателями – на 41% эффективнее снижает воспаление и на 43% снижает кровоточивость дёсен.
Источники:
- Роль противовоспалительного ополаскивателя в лечении заболеваний пародонта (Л.Ю. Орехова, А.А. Леонтьев, С.Б. Улитовский) Л.Ю. ОРЕХОВА, д.м.н., проф., завкафедрой; А.А. ЛЕОНТЬЕВ, врач-стоматолог; С.Б. УЛИТОВСКИЙ, д.м.н., проф. Кафедра терапевтической стоматологии СПб ГМУ им. акад. И. П. Павлова
- Использование адгезивного бальзама «Асепта®» при лечении воспалительных заболеваний пародонта Л.Ю. ОРЕХОВА*, д-р мед. наук, профессор, завкафедрой В.В. ТЭЦ**, д-р мед. наук, профессор, завкафедрой С.Б. УЛИТОВСКИЙ*, д-р мед. наук, профессор А.А. ЛЕОНТЬЕВ*, врач-стоматолог А.А. ДОМОРАД**, О.М. ЯКОВЛЕВА** СПбГМУ им. акад. И.П. Павлова, Санкт-Петербург — *Кафедра терапевтической стоматологии, **Кафедра микробиологии
- https://cyberleninka.ru/article/v/puti-sovershenstvovaniya-pervichnoy-profilaktiki-zabolevaniy-parodonta Острый герпетический стоматит у детей, Баранаева Е.А. Меркулова Е.П. журнал «Медицина и Здравоохранение»
- https://cyberleninka.ru/article/v/osobennosti-protivoretsidivnogo-lecheniya-allergicheskogo-stomatita Острые стоматиты у детей, Дроботько Л.Н., Страхова С.Ю.
Применение в период беременности и лактации
Адекватных и контролируемых исследований применения флуконазола у беременных женщин не проводилось. Описано несколько случаев множественных врождённых пороков у новорождённых, матери которых на протяжении большей части или всего первого триместра получали терапию флуконазолом в высокой дозе (400-800 мг/сут). Были отмечены следующие нарушения развития: брахицефалия, нарушение развития лицевой части черепа, нарушение формирования свода черепа, волчья пасть, искривление бедренных костей, истончение и удлинение ребер, артрогрипоз и врождённые пороки сердца. В настоящее время нет доказательств связи перечисленных врождённых аномалий с применением низких доз флуконазола (150 мг однократно для лечения вульвовагинального кандидоза) в первом триместре беременности.
Во время беременности применения флуконазола следует избегать, за исключением случаев тяжелых и потенциально угрожающих жизни грибковых инфекций, когда ожидаемая польза лечения для матери превышает возможный риск для плода. Женщинам детородного возраста следует использовать средства контрацепции.
Поскольку концентрация флуконазола в грудном молоке и в плазме одинакова, применять препарат в период грудного вскармливания противопоказано.
Флуконазол-OBL, 150 мг, капсулы, 4 шт.
При одновременном применении с варфарином флуконазол повышает протромбиновое время (на 12%), в связи с чем возможно развитие кровотечений (гематомы, кровотечения из носа и ЖКТ, гематурия, мелена). У пациентов, получающих кумариновые антикоагулянты, необходимо постоянно контролировать протромбиновое время.
После приема внутрь мидазолама флуконазол существенно увеличивает концентрацию мидазолама и психомоторные эффекты, причем это влияние более выражено после приема флуконазола внутрь, чем при его применении в/в. При необходимости сопутствующей терапии бензодиазепинами пациентов, принимающих флуконазол, следует наблюдать с целью соответствующего снижения дозы бензодиазепина.
При одновременном применении флуконазола и цизаприда возможны нежелательные реакции со стороны сердца, в т.ч. мерцание/трепетание желудочков (ари). Применение флуконазола в дозе 200 мг 1 раз/сут и цизаприда в дозе 20 мг 4 раза/сут приводит к выраженному увеличению плазменных концентраций цизаприда и увеличению интервала QT на ЭКГ. Одновременный прием цизаприда и флуконазола противопоказан.
У пациентов после трансплантации почки применение флуконазола в дозе 200 мг/сут приводит к медленному повышению концентрации циклоспорина. Однако при многократном приеме флуконазола в дозе 100 мг/сут изменения концентрации циклоспорина у реципиентов костного мозга не наблюдалось. При одновременном применении флуконазола и циклоспорина рекомендуется мониторировать концентрацию циклоспорина в крови.
Многократное применение гидрохлоротиазида одновременно с флуконазолом приводит к увеличению концентрации флуконазола в плазме на 40%. Эффект такой степени выраженности не требует изменения режима дозирования флуконазола у пациентов, получающих одновременно диуретики, однако следует это учитывать.
При одновременном применении комбинированного перорального контрацептива с флуконазолом в дозе 50 мг существенного влияния на уровень гормонов не установлено, тогда как при ежедневном приеме 200 мг флуконазола AUC этинилэстрадиола и левоноргестрела увеличиваются на 40% и 24% соответственно, а при приеме 300 мг флуконазола 1 раз в неделю — AUC этинилэстрадиола и норэтиндрона возрастают на 24% и 13% соответственно. Таким образом, многократное применение флуконазола в указанных дозах вряд ли может оказать влияние на эффективность комбинированного перорального контрацептива.
Одновременное применение флуконазола и фенитоина может сопровождаться клинически значимым повышением концентрации фенитоина. При данной комбинации следует контролировать концентрацию фенитоина и соответствующим образом скорректировать его дозу с целью обеспечения терапевтической концентрации в сыворотке крови.
Одновременное применение флуконазола и рифабутина может привести к повышению сывороточных концентраций последнего. При одновременном применении флуконазола и рифабутина описаны случаи увеита. Больных, одновременно получающих рифабутин и флуконазол, необходимо тщательно наблюдать.
Одновременное применение флуконазола и рифампицина приводит к снижению AUC на 25% и длительности T1/2 флуконазола на 20%. У пациентов, одновременно принимающих рифампицин, необходимо учитывать целесообразность увеличения дозы флуконазола.
Флуконазол при одновременном приеме приводит к увеличению T1/2 пероральных препаратов сульфонилмочевины (хлорпропамида, глибенкламида, глипизида и толбутамида). Больным сахарным диабетом можно назначать совместно флуконазол и пероральные препараты сульфонилмочевины, но при этом следует учитывать возможность развития гипогликемии.
Одновременное применение флуконазола и такролимуса приводит к повышению плазменных концентраций последнего. Описаны случаи нефротоксичности. При данной комбинации следует тщательно контролировать состояние пациентов.
При одновременном применении азольных противогрибковых средств и терфенадина возможно возникновение серьезных аритмий в результате увеличения интервала QT. При приеме флуконазола в дозе 200 мг/сут увеличения интервала QT не установлено, однако применение флуконазола в дозах 400 мг/сут и выше вызывает значительное увеличение концентрации терфенадина в плазме. Одновременный прием флуконазола в дозах 400 мг/сут и более с терфенадином противопоказан. Лечение флуконазолом в дозах менее 400 мг/сут в сочетании с терфенадином следует проводить под тщательным контролем.
При одновременном применении с флуконазолом в дозе 200 мг в течение 14 дней средняя скорость плазменного клиренса теофиллина снижается на 18%. При назначении флуконазола больным, принимающим теофиллин в высоких дозах, или больным с повышенным риском развития токсического действия теофиллина следует наблюдать за появлением симптомов передозировки теофиллина и, при необходимости, скорректировать терапию соответствующим образом.
При одновременном применении с флуконазолом отмечается повышение концентраций зидовудина, которое, вероятно, обусловлено снижением метаболизма последнего до его главного метаболита. До и после терапии с применением флуконазола в дозе 200 мг/сут в течение 15 дней больным СПИД и ARC (комплекс, связанный со СПИД) установлено значительное увеличение AUC зидовудина (20%).
При применении у ВИЧ-инфицированных пациентов зидовудина в дозе 200 мг каждые 8 ч в течение 7 дней в сочетании с флуконазолом в дозе 400 мг/сут или без него с интервалом в 21 день между двумя схемами, установлено значительное увеличение AUC зидовудина (74%) при одновременном применении с флуконазолом. Пациентов, получающих такую комбинацию, следует наблюдать с целью выявления побочных эффектов зидовудина.
Одновременное применение флуконазола с астемизолом или другими препаратами, метаболизм которых осуществляется изоферментами системы цитохрома Р450, может сопровождаться повышением сывороточных концентраций этих средств. При таких комбинациях следует тщательно контролировать состояние пациентов.
Особые указания
Лечение флуконазолом можно начинать до получения результатов посева и других лабораторных анализов, но после получения результатов этих исследований терапию необходимо изменить соответствующим образом.
В ходе лечения необходимо контролировать показатели крови, функцию почек и печени. При возникновении нарушений функций почек и печени следует прекратить прием препарата.
Лечение необходимо продолжать до появления клинической и гематологической ремиссии (исключением является острый влагалищный кандидоз). Преждевременное прекращение лечения приводит к рецидивам.
Больные СПИДом более склонны к развитию тяжелых кожных реакций при применении многих препаратов. В тех случаях, когда у больных с поверхностной грибковой инфекцией развивается сыпь и она расценивается как определенно связанная с флуконазолом, препарат следует отменить. При появлении сыпи у больных с инвазивными / системными грибковыми инфекциями, их следует тщательно наблюдать и отменить флуконазол при появлении буллезных изменений или многоформной эритемы.
В редких случаях применение флуконазола сопровождалось токсическими изменениями печени, в том числе с летальным исходом, главным образом у больных с серьезными сопутствующими заболеваниями. В случае гепатотоксических эффектов, связанных с флуконазолом, не отмечено явной зависимости их от общей суточной дозы, длительности терапии, пола и возраста больного. Гепатотоксическое действие флуконазола обычно было обратимым; признаки его исчезали после прекращения терапии. При появлении клинических признаков поражения печени, которые могут быть связаны с флуконазолом, препарат следует отменить.