НРК — это один из способов наращивания кости перед имплантацией. К операции прибегают для гарантии первичной стабильности импланта и исключения риска отторжения титанового корня, развития воспаления ткани. Недостаток кости восполняется костным заменителем, который закрепляется мембраной. Используют собственные или синтетические материалы. Метод безопасен: хирургическое вмешательство организуют под местной анестезией, делают небольшие разрезы тканей, производят подсадку костного материала, контролируют процесс приживления трансплантата.
Что такое направленная костная регенерация
Направленная костная регенерация — это операция по возмещению недостатка костной ткани заменителем, который закрепляют барьерной мембраной. После процедуры вокруг трансплантата образуется каркас (его формируют сосуды и клетки-остеоциты, которые продуцируют новую ткань). Натуральная кость постепенно заменяет искусственный материал.
Наращивание методом НРК производят по классическим параметрам:
- толщина вестибулярной костной стенки (у щеки) — до 2-2,5 мм;
- толщина кости между имплантатом и корнем соседней единицы — до 2,5-3 мм;
- толщина костной стенки между двумя титановыми корнями — до 3 мм.
Показания
Операция позволяет нарастить «нужный» объем для проведения качественной классической имплантации, способствует восстановлению функций челюсти, возвращает десне привлекательный облик.
Кость наращивают «с запасом», поскольку после операции поверхностные слои будут снабжены небольшим объемом кислорода по причине их меньшего кровообращения. Поэтому рассчитывают рассчитывают объем неизбежной резорбции ткани.
Помимо имплантации, показаниями к НРК являются:
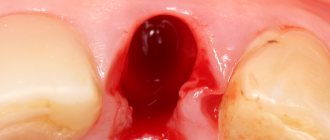
- быстрое восстановление физиологических параметров после удаления зуба;
- врожденная или приобретенная дефектность кости вокруг зубов;
- профилактика смещения зубов, их расшатывания, выпадения при заболеваниях тканей пародонта.
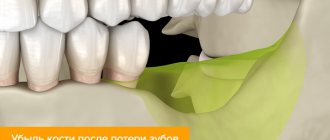
Почему происходит атрофия?
Какие костные материалы применяются
Остеопластика предполагает использование материалов, заменяющих кость. Ранее использовались трансплантаты, которые не получили широкого применения по причине частых отторжений чужеродного материала:
- Аллотрансплантанты
— донорская кость других людей. Материал получали от трупов, обрабатывали, стерилизовали, хранили в банках костной ткани. - Ксенотрансплантаты
— кости животных (крупного рогатого скота, свиней). Материал освобождали от белков методом нагревания (для исключения вероятности аллергической реакции после пересадки).
Мы не применяем устаревшие методики. Сейчас разработано множество синтетических компонентов, способствующих росту собственной кости, которые мы используем для наращивания костной ткани.
Синтетические материалы имеют высокую степень сродства и совместимости с натуральной костью, являются ее аналогами. Это гранулированные составы на базе:
- фосфатов кальция;
- хондроитин-сульфата;
- биостекла.
Эффективность и безопасность искусственных материалов подтверждена многочисленными исследованиями. Они просты в применении, хорошо приживаются, способствуют регенерации собственной кости, гипоаллергенны.
При остеопластике возможна комбинация искусственного заменителя и собственной кости человека в форме стружки (аутотрансплантат). Методика помогает сохранить объем заложенной костной ткани и ускорить темпы восстановления. Этот же метод выручает, если предстоит нарастить большой объем ткани.
При небольшом дефиците можно обойтись только синтетическими материалами.
Виды мембран
Мембранная техника, которую использует хирург, нужна для изоляции пространства от фиброзной ткани — создания условий для нормальной регенерации ткани. К мембранам предъявляют несколько требований:
- биологическая совместимость;
- прочность;
- предупреждение миграции клеток эпителия;
- соответствующий период резорбции.
В практике применяют два типа мембран:
- Резорбируемые.
Самостоятельно рассасываются через 6-24 недель после наращивания. Мембраны применяют при небольших дефектах (когда нужно нарастить не больше 2 мм) — они не так хорошо держат форму, как следующий вид. - Нерезорбируемые.
Не рассасываются — их устраняют через несколько месяцев после операции.
Для быстрого срастания искусственного материала с костной тканью челюсти в ряде случаев используют мембраны из плазмы крови пациента.
Стоматологическая имплантология является относительно молодой, но быстроразвивающейся наукой. Активно разрабатываются и внедряются новые виды дентальных имплантатов, биокомпозиционных материалов, совершенствуются способы операций [8, 9, 17, 19, 21, 26, 27, 34].
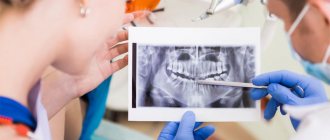
При планировании дентальной имплантации необходимо правильно выбрать место установки имплантата, тип имплантационной системы, оценить возможное количество устанавливаемых имплантатов. Решающее значение имеет костная структура челюстей, о достоверном состоянии которой можно судить только по результатам лучевых методов исследования. На предоперационном этапе чрезвычайно важно правильно определить размеры альвеолярного отростка верхней челюсти или альвеолярной части нижней челюсти, вид адентии, выявить степень атрофии костной ткани челюстей, оценить ее архитектонику и плотность для решения основных задач планирования дентальной имплантации и прогнозирования последующего лечения [16, 24, 34, 35].
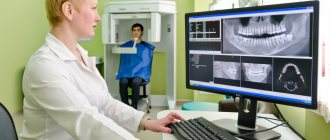
С помощью современных специализированных программ мультиспиральной компьютерной томографии (МСКТ) стало возможным получение дентальных объемных томограмм, что позволяет в сложных ситуациях правильно спланировать операцию имплантации, выбрать оптимальные имплантаты и математически рассчитать места их установки [22-24, 30, 34].
Активное развитие имплантологии показало, что на результаты лечения влияют не только знания и умение врача в постановке диагноза, предоперационном планировании и проведении дентальной имплантации, но и обоснованный выбор эффективной и безопасной поддерживающей лекарственной терапии.
Назначение курса антибактериальной терапии, противовоспалительных и десенсибилизирующих препаратов стало традиционным и обязательным в схеме послеоперационного лечения пациентов.
В амбулаторной стоматологической практике для проведения комплексной терапии воспалительных процессов и болевых синдромов челюстно-лицевой области, а также для превентивной аналгезии перед выполнением операций и травматичных вмешательств наиболее часто используются нестероидные противовоспалительные средства [4, 5, 7, 10, 11, 20, 29, 33, 37]. Хирургическая травма при проведении имплантации сопровождается повреждением тканей альвеолярного отростка, что провоцирует запуск цитокинового каскада (интерлейкины, колониестимулирующие факторы, интерфероны, фактор некроза опухоли -альфа, -бета, фактор тканевого роста -бета) и развитие воспалительной реакции. Избыточная продукция провоспалительных цитокинов может приводить к септическому состоянию раны, а также к генерализации воспалительного процесса и развитию органных дисфункций. Использование перед операцией противовоспалительных препаратов снижает образование провоспалительных цитокинов, что способствует уменьшению послеоперационной, краниофациальной и зубной боли, отека и воспаления. Однако при использовании нестероидных противовоспалительных средств возможно развитие побочных реакций. Эти препараты оказывают негативное влияние на слизистую оболочку желудочно-кишечного тракта, приводящее к развитию язвенных процессов, снижают агрегацию тромбоцитов, увеличивая возможность кровотечения, предрасполагают к развитию бронхоспазма, аллергических реакций, снижению диуреза, появлению отеков [2, 4, 31, 32, 40].
По статистике в последнее время происходит рост осложнений от традиционно применяемых для переоперационной медикаментозной терапии лекарств и значительное увеличение числа пациентов, имеющих противопоказания к их применению.
Рост осложнений от лекарственной терапии побуждает искать альтернативные методы лечения, одним из которых является гомеопатия. Интеграции гомеопатии в медицинскую практику способствует создание комплексных гомеопатических препаратов, подбираемых не по принципу подобия, а по общепринятому в медицине и привычному для врача этиологическому и патогенетическому принципу.
За последние годы в комплексной терапии воспалительных процессов челюстно-лицевой области нашли применение комплексные гомеопатические препараты Траумель С, Остеохель С и Калькохель [1, 3, 6, 12-15, 18, 25].
Наиболее широкое применение в качестве противовоспалительного средства в разных областях медицины, в том числе и в стоматологии, имеет комплексный гомеопатический препарат Траумель С, содержащий в своем составе компоненты, влияющие на все звенья патогенеза воспалительно-гнойных процессов. Траумель С действует на процессы микроциркуляции, устраняет венозный стаз, улучшает клеточное дыхание и окислительно-восстановительные процессы, активирует иммунитет и противомикробную защиту организма, дает противовоспалительный эффект, стимулирует регенерацию тканей, уменьшает боль и устраняет последствия травматических повреждений тканей, что позволяет использовать его в комплексной фармакотерапии воспалительно-гнойных процессов и травм тканей челюстно-лицевой области [1, 4, 6, 12-15, 18, 25, 38].
Показано, что простагландины и другие метаболиты арахидоновой кислоты, повышая мобилизацию кальция из костной ткани, способствуют костной резорбции [28, 36, 39]. В связи с этим для ускорения регенерации и замедления процесса резорбции костной ткани в послеоперационную комплексную терапию вводили препараты Остеохель С и Калькохель. Остеохель С улучшает метаболизм костной ткани, оптимизирует кальциевый обмен, обладает противовоспалительным и болеутоляющим действием. Калькохель нормализует обмен веществ, оптимизирует использование кальция при синтезе костной ткани, оказывает противовоспалительное, болеутоляющее, успокаивающее действие [3, 15].
Так как практические врачи решают разные по клинической сложности задачи, необходимо совершенствование методов диагностики, создание стандартизированных схем обследования пациентов для планирования костно-реконструктивной операции при дефиците костной ткани, а также разработка схемы медикаментозного сопровождения при подготовке пациентов к операции и в послеоперационный период. Это позволит выбрать наиболее оптимальный хирургический метод, определить количество биоматериала и решить вопрос об этапности операций и медикаментозного сопровождения пациентов. Такая позиция должна использоваться в каждом индивидуальном случае пластики при дефиците костной ткани, что определит разные варианты операции. Поэтому требуются единые подходы к диагностике и разработке дифференцированных методов реконструкции при дефиците костной ткани для зубной имплантации, что и явилось целью настоящего исследования.
Материал и методы
Настоящее исследование основано на результатах проведенных в 2007-2011 гг. костно-пластических операций у 356 пациентов (215 женщин и 141 мужчина) в возрасте от 25 до 70 лет с дефицитом костной ткани альвеолярного отростка челюсти для установления внутрикостных зубных имплантатов. Пациентов с дефицитом костной ткани на верхней челюсти было 203, на нижней челюсти — 153. Для подготовки к оперативным вмешательствам проводилось комплексное обследование: клиническое, антропометрическое, рентгенологическое, исследование моделей челюстей. Учет функционального состояния организма позволяет осуществлять индивидуальный выбор методов предоперационной подготовки в зависимости от наличия у пациента сопутствующих болезней и состояния иммунного статуса.
Наряду с клиническим обследованием планирование этапов лечения проводилось на основании данных лучевой диагностики. Нами проведена первичная оценка плотности костно-пластических материалов с помощью компьютерной томографии. Для оценки рентгенологической плотности костно-пластических материалов мы использовали МСКТ и ДОТ с оценкой результата по шкале Хаунсфилда.
Критерии оценки результатов традиционных рентгенологических методик были аналогичны для всех пациентов. Наиболее сложной задачей при планировании имплантации на нижней челюсти являлась оценка расположения нижнечелюстного канала.
При подготовке пациента к операции стоматологической имплантации в ряде случаев возникает необходимость выполнения дополнительных костно-реконструктивных операций с целью восстановления достаточного объема и формы альвеолярных отделов челюстей. Как правило, подобные ситуации связаны с атрофией альвеолярных гребней, постэкстракционными состояниями, реже — с неблагоприятными анатомическими условиями (например, критически низким расположением нижней стенки верхнечелюстной пазухи). Основными видами таких операций являются пластика с фиксацией трансплантационного материала «внакладку» и пластика с фиксацией материала внутрь кости. Также, по необходимости, может выполняться латерализация нижнего альвеолярного нерва или поднятие дна верхнечелюстной пазухи (открытый или закрытый синус-лифтинг). Кроме этого, использование костно-пластических материалов может быть необходимо при одномоментной операции имплантации или для заполнения околоимплантационного дефекта в лунке удаленного зуба. В качестве трансплантатов использовались ксеногенные костно-пластические материалы OsteoBiol — «Apatos», «Gen-os», «mp3», «Dual-Block», а также их сочетания. Для закрытия биоматериала и лучшей его адаптации к кости применялась мембрана «Evolution».
Изучены результаты 6 типов операций костной пластики: поднадкостничная трансплантация (1-я группа), накладная трансплантация с подготовкой кости (2-я группа), трансплантация биоматериала внутрь кости (3-я группа), реконструкция альвеолярного сегмента верхней челюсти доступом через альвеолярную дугу с поднятием дна верхнечелюстной пазухи (4-я группа), реконструкция альвеолярного отростка верхней челюсти доступом через переднелатеральную стенку с поднятием дна верхнечелюстной пазухи (5-я группа), реконструкция альвеолярного отростка и тела верхней челюсти доступом через дистально-латеральную стенку с поднятием дна верхнечелюстной пазухи (6-я группа).
Все операции проводили в амбулаторных условиях под проводниковой или инфильтрационной анестезией анестетиками амидного ряда с применением премедикации. Срок контрольного наблюдения составил от 1 года до 4 лет.
При проведении дентальной имплантации использовалась традиционная схема медикаментозной предоперационной подготовки и послеоперационного ведения пациентов, в которую были включены комплексные гомеопатические препараты.
В протокол предоперационной подготовки и послеоперационного лечения пациентам было включено курсовое применение (21 день) комплексных гомеопатических препаратов. Траумель С пациенты применяли как до проведения имплантации, так и в послеоперационном периоде, а Остеохель С и Калькохель — в послеоперационном периоде. Препараты назначали сублингвально по 1 таблетке 3 раза в день, не совмещая с приемом других лекарств или пищи.
Схема медикаментозной предоперационной подготовки и послеоперационного ведения пациентов
До операции
пациентам назначали антибактериальные и противовоспалительные средства.
В течение 7 дней до имплантации пациенты применяли сублингвально по 1 таблетке 3 раза в день комплексный гомеопатический препарат Траумель С.
Для профилактики инфекционных осложнений за 40-60 мин до операции пациентам назначали однократно антибиотик широкого спектра действия амоксициллин/клавуланат — 2 таблетки по 625 мг. При наличии противопоказаний к его применению можно использовать азитромицин в дозе 500 мг в сочетании с метронидазолом (500 мг) или кларитромицин (клацид) в дозе 500 мг в сочетании с метронидазолом (500 мг).
Для превентивной аналгезии за 30 мин до операции назначали нестероидный противовоспалительный препарат кетопрофен — 150 мг.
Для антисептической обработки тканей использовали 0,05% раствора хлоргексидина.
После операции
пациентам назначали противовоспалительные и болеутоляющие средства. Наиболее часто пациенты применяли кетопрофен — 150 мг 1 раз в сутки или 50 мг — 3 раза в сутки.
При наличии противопоказаний к применению кетопрофена можно использовать целекоксиб — 100 мг 2 раза в сутки или нимесулид — 100 мг 2 раза в сутки.
Всем пациентам назначали комплексные гомеопатические препараты.
Траумель С пациенты применяли сублингвально по 1 таблетке 3 раза в день в послеоперационном периоде до исчезновения признаков воспаления (около 2 нед).
Остеохель С назначали по 1 сублингвальной таблетке 3 раза в день со 2-й недели после операции, т.е. 1-я неделя его применения совпадала с последней неделей приема Траумеля С. Курс лечения составлял 21 день.
Калькохель пациенты применяли сублингвально по 1 таблетке 3 раза в день с 4-й послеоперационной недели, т.е. последняя неделя приема Остеохеля С совпадала с первой неделей приема Калькохеля. Курс лечения составлял 21 день.
Для антисептической обработки тканей применяли 0,05% раствора хлоргексидина и наносили метрогил дента на швы 3 раза в день после еды в течение 5-7 дней.
По показаниям назначались антимикробные химиотерапевтические препараты.
Амоксициллин/клавуланат в дозе 625 мг применяли 3 раза в сутки. При наличии противопоказаний к его применению назначали азитромицин 500 мг + метронидазол 500 мг 2 раза в сутки или кларитромицин 500 мг 2 раза в сутки + метронидазол 500 мг 2 раза в сутки. Длительность курса — 5 дней.
Для профилактики дисбактериоза при использовании антибиотиков в комплексную терапию вводили пробиотик линокс — по 2 капсулы 3 раза в сутки в течение 21 дня.
По показаниям в комплексную терапию вводили антигистаминный препарат лоратадин — 10 мг 1 раз в сутки в течение 5 дней.
Всем пациентам в протокол предоперационной подготовки и послеоперационного лечения включали препараты Траумель С, Остеохель С и Калькохель по предложенной нами схеме.
Результаты и обсуждение
Поднадкостничная трансплантация проведена у 67 пациентов. Показанием для операции являлись недостаточная высота и ширина кости альвеолярного отростка и снижение окклюзионной плоскости. Использовали ксеногенные костно-пластические материалы OsteoBiol — «Apatos», «Gen-os», «mp3», «Sp-Block», а также их сочетания. Предпочтение отдавали «mp3» за счет простоты и контролируемости введения материала и «Dual Block», обеспечивающему жесткость профиля создаваемого объема костного материала. Спустя 4-5 мес устанавливали имплантаты. Остеокондуктивные материалы к этому времени клинически и рентгенологически не реструктурировались в зрелую кость; остеоиндуктивные — представляли плотную минерализованную кость. Получен 93% успех у всех пациентов.
Накладная трансплантация с подготовкой кости проведена у 42 человек. Показанием для операции была недостаточная ширина альвеолярной дуги и атрофия передней поверхности альвеолярного отростка, что создавало невозможность установления имплантата в правильное положение в соответствии с окклюзией. Для данного типа операций предпочтение отдавали костному блоку «Dual Block», который обеспечивал создание жесткого профиля создаваемого объема костного материала и хорошо восстанавливал объем утраченной костной ткани с вестибулярной стороны альвеолярной части челюстей. Для лучшей фиксации костные блоки фиксировали костными винтами и закрывали мембраной «Evolution». Рентгенологически через 6 мес граница материнской кости и ремоделированного биоматериала не определялась.
У 2 больных в раннем послеоперационном периоде отмечалось расхождение единичных швов. Наличие мембраны позволило полностью сохранить костно-пластический материал. После лечения заживление раны завершалось благополучно. Имплантаты и зубные протезы с опорой на них функционировали хорошо. У 2 пациентов через 2-3 года за счет резцового перекрытия и функциональной перегрузки зубные протезы на имплантатах стали подвижны и были утрачены. У остальных 40 пациентов результаты операции хорошие.
Трансплантация биоматериала внутрь кости проведена у 41 пациента. Показанием к операции являлись узкая альвеолярная дуга и необходимость ее смещения в вестибулярную сторону для правильных окклюзионных взаимоотношений. Образовавшиеся пустоты заполняли биоматериалом, который закрывали мембраной «Evolution». Для данного типа операций предпочтение отдавали костно-пластическому материалу «Apatos», «Gen-os». Причем «Apatos» нами применялся у пациентов с 3-м и 4-м классом плотности костной ткани по Misch, что обеспечивало повышение плотности костного регенерата в последующем, а «Gen-os» у пациентов с 1-м классом плотности костной ткани, что позволяло получить костный регенерат меньшей плотности и создавало лучшую остеоинтеграцию дентальных имплантатов в последующем. Через 6 мес на рентгенограмме и МСКТ определялась кость плотного строения, имплантаты окружены и плотно сращены с костной тканью. У пациентов этой группы достигнут 96% успех операции.
Операция реконструкции альвеолярного сегмента верхней челюсти доступом через альвеолярную дугу с поднятием дна верхнечелюстной пазухи проведена у 52 больных. У всех пациентов функционирование имплантатов в протезных конструкциях проходило хорошо, у 4 человек спустя 1,5-2 года понадобилась смена зубного протеза.
Реконструкция альвеолярного отростка верхней челюсти доступом через переднелатеральную стенку с поднятием дна верхнечелюстной пазухи проведена у 46 пациентов. Анализируя ремоделирование биоматериала по рентгенограмме и МСКТ у 17 пациентов, мы отметили, что к концу 4-го месяца тень костного регенерата была расплывчатой, кортикальная пластинка у дна верхнечелюстной пазухи не просматривалась. К концу 6-го месяца отмечена плотная структура реорганизованной кости. У 29 пациентов с одномоментной костной пластикой и имплантацией рентгенологические исследования, в том числе МСКТ, показали, что кость через 6 мес имела плотное строение, рисунок кости был несколько смазан. Четко прослеживалась кортикальная пластинка как по альвеолярной дуге, так и обращенная к верхнечелюстной пазухе. В динамике плотность ремоделированной кости увеличивалась через 2 года. По данным МСКТ, массив кости уменьшился в среднем по высоте на 2 мм и остался неизменным по горизонтальной и сагиттальной плоскостям. У всех 46 пациентов с отсроченной и немедленной имплантацией получены положительные результаты.
Реконструкция альвеолярного отростка и тела верхней челюсти доступом через дистально-латеральную стенку с поднятием дна верхнечелюстной пазухи проведена 98 больным. Показаниями к операции являлись: малое количество кости в области моляров, пневматический тип верхнечелюстной пазухи с низким расположением бухт, в том числе в области бугра верхней челюсти. У 62 пациентов этой группы осуществлено двухэтапное вмешательство и у 36 — одноэтапная операция костной пластики с установлением имплантатов. У 14 больных окончательной минерализации материала через 12-18 мес не происходило. Вместе с тем функционирование имплантатов было хорошим.
Из 615 имплантатов 606 функционируют, 9 имплантатов были удалены через 2-3 года в связи с периимплантитом.
У пациентов 4-6-й групп при операциях нами использовался материал «mp3» как наиболее адаптированный для операций по поднятию дна верхнечелюстной пазухи. Костное окно закрывали мембраной «Evolution».
Традиционно рентгенологический контроль состояния области реконструктивно-восстановительной операции осуществляется дважды перед этапом установки имплантатов: сразу после выполнения реконструктивной операции и непосредственно перед дентальной имплантацией (как правило, через 5-6 мес).
У 299 пациентов использовалась традиционная схема медикаментозной предоперационной подготовки и послеоперационного ведения, в которую были включены комплексные гомеопатические препараты. У 47 (13,6%) пациентов с небольшими объемами хирургических вмешательств и при наличии противопоказаний к применению антибиотиков назначение комплексных гомеопатических препаратов позволило полностью отказаться от использования химиотерапевтических средств.
Заключение
Традиционно считается, что установление имплантатов возможно только через 5-6 мес после пластики кости. Однако проведенный нами сравнительный анализ двухэтапной и одноэтапной операций костной пластики с немедленным и отсроченным установлением имплантатов показал одинаково хорошие результаты во всех группах.
Все используемые нами биоматериалы были эффективны с учетом выбора материала для конкретного клинического случая. Следует рекомендовать сочетание костно-пластического материала, особенно с аутокостью.
Эффективность операции реконструкции альвеолярного отростка челюстей и зубной имплантации определяли на основании следующих признаков:
— жалоб больного, в том числе на функцию зубного протеза с опорой на имплантат;
— клинической оценки зубного протеза с опорой на имплантат;
— состояния слизистой оболочки у шейки имплантата, плотности ее, глубины кармана, наличия кровоточивости при погружении зонда;
— рентгенологической картины кости вокруг имплантата;
— рентгенологической картины ремоделированной кости;
— состояния верхнечелюстной пазухи в соответствии с жалобами больного и состояния верхнечелюстной пазухи в рентгеновском отображении;
— индекса гигиены полости рта.
Критерии оценки эффективности костно-реконструктивной операции в динамике были следующие:
— расположение костно-пластического материала по отношению к кортикальной пластинке альвеолярного гребня;
— прилегание костно-пластического материала к материнской кости;
— степень и темпы неоостеогенеза и резорбции костно-пластического материала;
— объем биоматериала (по сравнению с контрольным исследованием, выполненным сразу после костно-реконструктивной операции);
— структура, однородность и плотность костно-пластического материала в зависимости от его вида (соответствие с нормальными значениями).
Полученные результаты показали, что планирование и контроль эффективности костно-реконструктивных операций были наиболее успешны у пациентов 2-й и 3-й групп, где лучевое обследование проводилось с помощью высокотехнологичных методов, которые на этапе планирования позволили получить полную информацию о размерах и форме костных дефектов челюстей. Специализированное программное обеспечение дало возможность оценить необходимое количество костно-пластического материала для их возмещения.
Анатомо-клиническое исследование челюстей при дефиците костной ткани и объемная диагностика атрофии кости позволяют нам предложить различные методы наращивания кости и различные оперативные доступы. И только учитывая все особенности каждого костно-пластического материала (структуру, химический состав), сроки рассасывания, его рентгенологические характеристики и плотность, можно корректно проводить оценку эффективности выполняемых реконструктивных операций. Проведение предоперационной медикаментозной подготовки и индивидуальный выбор послеоперационной фармакотерапии снижают частоту послеоперационных осложнений и повышают эффективность дентальной имплантации.
Таким образом, индивидуальное планирование предстоящего вмешательства и его медикаментозного сопровождения позволяет получить хорошие результаты как при двухэтапной, так и при одноэтапной операции дентальной имплантации.
Этапы НРК
Операцию организуют под анестезией. Хирург действует по классическому алгоритму:
- Разрезает десну вдоль лунки потерянного зуба, делает несколько разрезов сбоку — отслаивает десневой лоскут.
- Фиксирует в оголенную кость имплант (если операцию организуют одновременно с имплантацией).
- Замещает недостающий объем трансплантатом, покрывает его мембраной с выступом на 2-3 мм за пределы костного материала. Если не исключает факт вдавливания мембраны внутрь дефекта, сверху накладывает титановую сетку.
- Закрепляет мембрану (швами или винтами).
- Сводит края раны, накладывает швы.
Операция длится 1-1,5 часа.
Техника проведения процедуры
Перед хирургическим вмешательством врач осматривает больного, изучает состояние ротовой полости. Дополнительно проводятся лабораторные исследования, которые помогут определить возможные противопоказания.
Некоторым пациентам может потребоваться лечение пародонта, других патологий, которые могут стать причиной осложнений в процессе восстановления после операции. Костная регенерация в стоматологии выполняется в 5 основных этапов:
- Обезболивание. Хирургическое вмешательство проводят под местной анестезией. По желанию больного врач может выполнить процедуру под общим наркозом.
- Когда начинается действие анестетика, десна разрезается в нескольких местах. Врач предварительно определяет места, где будет обнажаться кость. После разреза происходит отслоение лоскутов десны.
- В местах, где отсутствует костная ткань, врач делает наложение трансплантата. Материал костного заменителя предварительно согласовывается с пациентом. Сверху трансплантата выстилают биологическую мембрану.
- Мембрана надежно фиксируется при помощи швов, специальных винтов, которые используют в стоматологии.
- Ушивание отслоенных лоскутов десневой ткани, чтобы закрыть рану.
Процедура длится около 1,5-2 часов. При необходимости перед наложением мембраны врач может установить титановую сетку. Это нужно, чтобы предотвратить вдавливание мембраны при особенном анатомическом строении зубов у пациента.
Можно ли проводить одновременно с имплантацией
Две операции комбинируют в одну при соблюдении условий:
- форма дефекта позволяет правильно установить искусственный корень в любой из плоскостей;
- при установке имплантат находится в пределах костного контура (не выходит за касательную, проведенную к линии кости);
- устраняют горизонтальный (не вертикальный) дефект.
Вживленный имплант может стать барьером для роста кровеносных сосудов и тормозить формирование новой кости. Если имплантат выступает за контур костной ткани, не исключают риск получения сформировавшейся фиброзной ткани с включениями подсаженного материала.
Применяемые материалы
Установка имплантата позволяет восстановить корневую систему, однако для этого необходимо достаточно плотное основание, способное зафиксировать искусственный штифт, что и обуславливает необходимость использования остеоиндуктивных средств, стимулирующих регенерацию. Двухслойные коллагеновые мембраны, обработанные восстанавливающим препаратом, позволяют восстановить естественный цикл кровообращения. В качестве материала, используемого для изготовления мембран, применяются резорбируемые и нерезорбируемые элементы, отличающиеся функциональными свойствами. При направленной регенерации также применяются биоактивные соединения и дистрактирующие составы – для получения оптимальной комбинации врачи сочетают различные элементы, способствующие ускорению интеграции.