Нимесил и Кеторол являются медикаментами, помогающими избавиться от воспалительных процессов, интенисвных болевых ощущений. Оба лекарства относятся к группе нестероидных противовоспалительных средств. Перед выбором подходящего варианта рекомендуется проконсультироваться с врачом.
Нимесил и Кеторол являются медикаментами, помогающими избавиться от воспалительных процессов, интенисвных болевых ощущений.
Отличия
Кеторол чаще применяется в качестве обезболивающего: его эффективность при воспалениях ниже, чем у Нимесила, поэтому доктора назначают более действенное лекарство. Нимесил может быть использован в качестве комплексного средства; он хорошо помогает и при болезненности, и при инфекционных процессах, сопровождающихся гипертермией.
Различны формы выпуска. Кеторол можно приобрести в виде таблеток или раствора для внутримышечных инъекций. Нимесил продают в виде порошка для изготовления раствора для перорального применения.
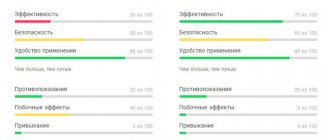
Нимесил реже вызывает побочные реакции. Это часто учитывают при выборе средства для обезболивания.
Лекарства обладают разным принципом действия. Кеторол подавляет активность ферментов первого и второго типа, синтезирующих простагландины. Подобное воздействие, однако, может негативно повлиять на функционирование органов желудочно-кишечного тракта. Второй препарат оказывает воздействие только на ферменты второго типа; обезболивающий эффект при этом становится менее выраженным.
НПВП и триптаны при мигрени: раздельно или вместе?
Согласно международным рекомендациям, лечение приступа мигрени у большинства пациентов должно начинаться с применения ненаркотического анальгетика или нестероидного противовоспалительного препарата (НПВП). Плацебо–контролируемые исследования при мигрени были проведены для ацетилсалициловой кислоты (АСК) [1–4], ибупрофена [5,6], диклофенака [7–9], метамизола [10], феназона [11], толфенамовой кислоты [12], парацетамола [13]. Показано, что комбинация АСК с парацетамолом и кофеином высокоэффективна при мигрени и имеет преимущества перед отдельно применяемыми компонентами [14–16]. Внутривенно вводимая АСК купирует приступ мигрени лучше, чем подкожно вводимый эрготамин [17]. Комбинация АСК с метоклопрамидом была так же эффективна, как суматриптан [18]. Шипучая АСК (1000 мг), ибупрофен (400 мг) и суматриптан (50 мг) были одинаково эффективны при мигрени [19,20]. В плацебо–контролируемом исследовании показано, что калиевая соль диклофенака в виде саше (50 и 100 мг) при купировании мигрени была эффективна как суматриптан (100 мг) [9]. Селективный ингибитор ЦОГ 2–го типа вальдекоксиб (20–40 мг) также уменьшал боль при мигрени [21]. Европейская Федерация Неврологических Сообществ (EFNS) рекомендует для лечения мигрени применять НПВП, эффективность которых доказана в рандомизированных двойных слепых, плацебо–контролируемых исследованиях [22] (табл. 1). Для купирования мигрени в первую очередь рекомендованы НПВП с быстрым накоплением в плазме (Tmax) и коротким периодом полувыведения (T1/2), что обеспечивает скорое развитие анальгезии и безопасность препарата при его повторном применении. Для этой цели созданы препараты с измененными физико–химическими и фармакокинетическими свойствами, благодаря которым можно добиться быстрой анальгезии (табл. 2). Для лечения мигрени наиболее часто используются диклофенак, кетопрофен, кеторолак и ибупрофен, поскольку их анальгетическая активность выше, чем у других НПВП [23]. Например, после внутримышечного введения натриевой соли диклофенака (75 мг) или после приема внутрь саше калиевой соли диклофенака (Вольтарен–рапид 50 мг) анальгезия наступает в среднем через 15 мин. Входящие в состав саше анисовый и ментоловый ароматизаторы улучшают органолептические свойства препарата и уменьшают тошноту. В большом рандомизированном исследовании показано, что при лечении многих приступов мигрени эффективность калиевой соли диклофенака в отношении головной боли сравнима с суматриптаном, а сопутствующие тошнота и рвота уменьшались достоверно чаще, чем при использовании триптана [9] (табл. 3). Клиническая эффективность триптанов при мигрени доказана в больших плацебо–контролируемых исследованиях, которые отражены в нескольких опубликованных сравнительных анализах. Триптаны эффективны в любой период приступа мигрени, однако их раннее применение повышает эффективность лечения [3,15,18]. Применение триптанов в фазу ауры до появления головной боли неэффективно. Накопленный опыт долгосрочного применения триптанов свидетельствует, что их не следует применять более 9 дней в месяц, так как это достоверно повышает риск перехода эпизодической формы мигрени в хроническую и способствует развитию абузусной головной боли. Различия в клинической эффективности триптанов определяются не только фармакологическими параметрами препаратов, но и индивидуальной чувствительностью пациента. В связи с этим при отсутствии эффекта от применения одного триптана не следует отказываться в следующий раз от использования другого. Анализ 53 исследований показывает, что эффективность триптанов принятых внутрь примерно одинакова, и только элетриптан в дозе 80 мг обладает большей эффективностью как в целом, так и в первые 30 мин. после приема препарата. Сравнительный анализ применения различных лекарственных форм триптанов показывает, что интраназальное и ректальное применение этих препаратов особенно перспективно при сопутствующей рвоте. Европейская федерация неврологических сообществ (EFNS) рекомендует для лечения мигрени применять триптаны, эффективность которых неоднократно доказана в рандомизированных двойных слепых, плацебо–контролируемых исследованиях [22] (табл. 4). В последнее время активно обсуждается и изучается возможность и целесообразность комбинированного использования НПВП и триптана для лечения мигрени. Результаты проведенного в 2005 г. исследования показали, что фиксированная комбинация суматриптана (50 мг) и напроксена натрия (500 мг) более эффективна при купировании приступа мигрени, чем монотерапия этими препаратами [24]. Головная боль через 2 ч уменьшалась значительно больше у пациентов, принимавших фиксированную комбинацию суматриптана с напроксеном (65%), чем у больных, получавших монотерапию суматриптаном (49%) или напроксеном (46%) (p<0,01). Полное купирование головной боли в этом исследовании зарегистрировано у 29% принимавших фиксированную комбинацию сумартриптана и напроксена, 25% принимавших суматриптан и 17% принимавших напроксен (p<0,001). Сравнительная эффективность ризатриптана (10 мг) и его комбинированное применение с рофекоксибом (25 мг) была изучена у 56 пациентов с мигренью. В этом открытом исследовании не было показано статистически значимой разницы между группами лечения в отношении купирования боли и сопутствующих симптомов тошноты, рвоты, свето– и звукобоязни. Однако число пациентов c рецидивами головной боли после ее удачного купирования было достоверно (p<0,001) меньшим в группе больных принимавших комбинацию рофекоксиба и ризатриптана (20%), чем в группе принимавших только ризатриптан (53%). Авторы не обнаружили различий между группами в частоте развития побочных эффектов [25]. Еще одно исследование было посвящено сравнительной эффективности ризатриптана (10 мг) и его комбинации с рофекоксибом (50 мг) и толфенамовой кислотой (200 мг) при лечении шести последовательных приступов мигрени у 45 пациентов. Полное купирование боли через 2 ч было зарегистрировано у 37,9% больных, получавших монотерапию ризатриптаном, у 40,6% – комбинированное лечение ризатриптаном и толфенамовой кислотой и у 62,9% комбинированное лечение ризатриптаном и рофекоксибом. Однако через 4 ч после примененного лечения различий между группами уже не было. Число случаев возврата мигрени после удачного купирования было меньшим при комбинированном применении триптана с НПВП (15,4% для комбинации с рофекоксибом и 7,7% для комбинации с толфенамовой кислотой), чем при монотерапии ризатриптаном (50%) [26]. В 2007 г. было закончено исследование, подтвердившее высокую эффективность комбинации суматриптана (85 мг) и напроксена (500 мг) при лечении приступа мигрени [27]. Авторы этих и других исследований предполагают, что преимущество комбинации триптана и НПВП обусловлено комплексным воздействием этих препаратов на различные механизмы патогенеза мигрени, а также различиями в фармакокинетике этих классов препаратов. Подчеркивается целесообразность применения НПВП в фазу ауры, когда триптаны не рекомендованы, или раннего совместного применения у пациентов с тяжелым течением мигрени. Благодаря комбинированному применению НПВП и триптана удается ускорить время наступления анальгезии, а также предупредить рецидив мигрени (рис. 1). Накопленные данные позволяют сформулировать ряд положений, которые помогут повысить эффективность лечения приступа мигрени: 1. НПВП эффективны при мигрени и могут рекомендованы для большинства больных в качестве препаратов первого выбора. Введение НПВП внутримышечно или в виде модифицированной формы саше обеспечивает более быстрое развитие анальгезии. Если пациент не может отличить приступ мигрени от головной боли напряжения, то ему следует принять НПВП. 2. Триптаны являются высокоэффективными средствами лечения мигрени. Они действуют на основные звенья патогенеза мигрени и не являются анальгетиками. Их не следует принимать во время мигренозной ауры. Триптаны, у больных не отвечающих на терапию НПВП, являются препаратами первого выбора. Существует индивидуальная чувствительность пациентов к тому или иному триптану. 3. Комбинированное применение НПВП и триптана позволяет более эффективно купировать головную боль и предупредить рецидив мигрени. 4. При выраженной тошноте и рвоте следует избегать приема НПВП и триптанов внутрь. Предпочтительны интраназальный, ректальный или внутримышечный пути введения.
Литература 1. Chabriat H, Joire JE, Danchot J, Grippon P, Bousser MG. Combined oral lysine acetylsalicylate and metoclopramide in the acute treatment of migraine: a multicentre double–blind placebo– controlled study. Cephalalgia 1994; 14: 297–300. 2. Nebe J, Heier M, Diener HC. Low–dose ibuprofen in self–medication of mild to moderate headache: a comparison with acetylsalicylic acid and placebo. Cephalalgia 1995; 15: 531–535. 3. Tfelt–Hansen P., Henry P., Mulder L.J., Scheldewaert R.G., Schoenen J., Chazot G. The effectivenes of combined oral lysine acetilsalicylate and metoclopramide compared with oral sumatriptan for migraine // Lancet. – 1995. – Vol. 346. – P.923–926. 4. Diener HC, Bussone G, de Liano H, et al. Placebo controlled comparison of effervescent acetylsalicylic acid, sumatriptan and ibuprofen in the treatment of migraine attacks. Cephalalgia 2004; 24: 947–954. 5. Havanka–Kanniainen H. Treatment of acute migraine attack: ibuprofen and placebo compared. Headache 1989; 29: 507–509. 6. Kloster R, Nestvold K, Vilming ST. A double–blind study of ibuprofen versus placebo in the treatment of acute migraine attacks. Cephalalgia 1992; 12: 169–171 7. Karachalios GN, Fotiadou A, Chrisikos N, Karabetsos A, Kehagioglou K. Treatment of acute migraine attack with diclofenac sodium: a double–blind study. Headache 1992; 32: 98–100. 8. Dahlof C., Bjorkman R. Diclofenac–K (50 and 100 mg) and placebo in the acute treatment of migraine. Cephalalgia 1993; 13: 117–123. 9. The Diclofenac–K/Sumatriptan Migraine Study Group. Acute treatment of migraine attacks: efficacy and safety of a nonsteroidal antiinflammatory drug, diclofenacpotassium, in comparison to oral sumatriptan and placebo. Cephalalgia 1999; 19: 232– 240 10. Tulunay FC, Ergun H, Gulmez SE, et al. The efficacy and safety of dipyrone (Novalgin) tablets in the treatment of acute migraine attacks: a double–blind, crossover, randomized, placebo–controlled, multi–center study. Funct Neurol 2004; 19: 197–202 11. Goebel H, Heinze A, Niederberger U, Witt T, Zumbroich V. Efficacy of phenazone in the treatment of acute migraine attacks: a double–blind, placebo–controlled, randomized study. Cephalalgia 2004; 24: 888–893 12. Myllyla VV, Havanka H, Herrala L, et al. Tolfenamic acid rapid release versus sumatriptan in the acute treatment of migraine: comparable effect in a double–blind, randomized, controlled, parallel–group study. Headache 1998; 38: 201–207. 13. Lipton RB, Baggish JS, Stewart WF, Codispoti JR, Fu M. Efficacy and safety of acetaminophen in the treatment of migraine: results of a randomized, double–blind, placebo–controlled, population–based study. Arch Intern Med 2000; 160: 3486–3492. 14. Lipton RB, Stewart WF, Ryan RE, Saper J, Silberstein S, Sheftell F. Efficacy and safety of acetaminophen, aspirin, and caffeine in alleviating migraine headache pain – three double–blind, randomized, placebo–controlled trials. Arch Neurol 1998; 55: 210–217 15. Diener H.C., Pfaffenrath V, Pageler L. The fixed combination of acetylsalicylic acid, paracetamol and caffeine is more effective than single substances and dual combination for the treatment of headache: a multi–centre, randomized, double–blind, single–dose, placebo–controlled parallel group study. Cephalalgia 2005; 25: 776–787. 16. Goldstein J, Silberstein SD, Saper JR, Ryan RE Jr, Lipton RB. Acetaminophen, aspirin, and caffeine in combination versus ibuprofen for acute migraine: results from a multicenter, double–blind, randomized, parallelgroup, single–dose, placebo–controlled study. Headache 2006; 46: 444–453 17. Limmroth V, May A, Diener HC. Lysine–acetylsalicylic acid in acute migraine attacks. Eur Neurol 1999; 41: 88–93. 18. Tfelt–Hansen P., Henry P., Mulder L.J., Scheldewaert R.G., Schoenen J., Chazot G. The effectivenes of combined oral lysine acetilsalicylate and metoclopramide compared with oral sumatriptan for migraine // Lancet. – 1995. – Vol. 346. – P.923–926. 19. Diener HC, Eikermann A, Gessner U, et al. Efficacy of 1000 mg effervescent acetylsalicylic acid and sumatriptan in treating associated migraine symptoms. Eur Neurol 2004; 52: 50–56 20. Lampl C, Voelker M, Diener HC. Efficacy and safety of 1000 mg effervescent aspirin: individual patient data meta–analysis of three trials in migraine headache and migraine accompanying symptoms. J Neurol 2007; 254: 705–712. 21. Kudrow D, Thomas HM, Ruoff G, et al. Valdecoxib for treatment of a single, acute, moderate to severe migraine headache. Headache 2005; 45: 1151–1162 22. Evers, S., Afra, J., Frese, A., Goadsby P. J., Lindе M., May A. and Sandor P. S. EFNS guideline on the drug treatment of migraine – revised report of an EFNS task force. European Journal of Neurology 2009, 16, 968–981 23. Игнатов Ю.Д., Кукес В.Г., Мазуров В.И. Клиническая фармакология нестероидных противовоспалительных средств, М., ГЭОТАР, 2010,–258 С 24. Smith TR, Sunshine A, Stark SR, et al. Sumatriptan and naproxen sodium for the acute treatment of migraine. Headache 2005; 45:983–991. 25. Krymchantowski AV, Barbosa JS. Rizatriptan combined with rofecoxib vs. rizatriptan for the acute treatment of migraine: an open label pilot study. Cephalalgia 2002;22:309–12. 26. Krymchantowski AV, Bigal ME. Rizatriptan versus rizatriptan plus rofecoxib versus rizatriptan plus tolfenamic acid in the acute treatment of migraine. BMC Neurol 2004;4:10 27. Brandes JL, Kudrow D, Stark SR, et al. Sumatriptan–naproxen for acute treatment of migraine: a randomized trial. JAMA 2007; 297:1443–1454
Противопоказания
Нельзя использовать для лечения Нимесил при непереносимости компонентов, аллергических реакциях, воспалительных процессах в кишечнике, лихорадке, при вирусных патологиях, бронхиальной астме, рецидивирующем образовании полипов в полостях носа, язвенной болезни желудка или двенадцатиперстной кишки, тяжелой почечной, печеночной или сердечной недостаточности, любых патологиях печени. Запрещен прием во время беременности, лактации. Детям нельзя принимать до 12 лет. Не использовать при алкогольной, наркотической зависимостях. Не сочетать с другими НПВС.
Лечиться Кеторолом нельзя при непереносимости компонентов, аллергии, язвенной болезни двенадцатиперстной кишки и желудка, желудочных кровотечениях, воспалительных процессах в кишечнике, гемофилии, нарушениях свертываемости крови, сердечной, почечной, печеночной недостаточности, патологиях печени и почек в активной стадии, после аортокоронарного шунтирования, перед и в процессе хирургического вмешательства, при беременности, лактации, во время родов. Детям не применять до 16 лет. Не сочетать с другими НПВС, содержащими ацетилсалициловую кислоту.
Восстановление сразу после операции
В первые дни после операции мы рекомендуем своим пациентам по возможности не выезжать в другой город. Находясь вблизи к стоматологии, вы при необходимости своевременно получите медицинскую помощь.
Итак, вы отправились домой после имплантации зубов. Вы можете чувствовать небольшую слабость, онемение от анестезии и незначительный дискомфорт в области вмешательства. Это состояние пройдет через 3-4 часа, поэтому вам не нужно принимать дополнительные меры.
Однако первые 1-2 дня вашему организму потребуется время на восстановление. Чтобы этот процесс прошел легко и незаметно для вашего привычного образа жизни, мы рекомендуем придерживаться следующих правил:
- Первые сутки ограничьтесь только полосканием ротовой полости. На следующий день уже можно чистить зубы щеткой и пастой, аккуратно минуя место установки импланта, чтобы не повредить шов.
- Прикладывайте прохладный компресс с наружной стороны имплантированной области. Это следует делать очень осторожно, чтобы избежать переохлаждения нерва рядом с имплантом.
- Первые дни необходимо принимать антибиотики, обезболивающее принимается по состоянию, если есть незначительная болезненность. Также необходимо предотвратить механическое воздействие в область имплантации
- Откажитесь от физических нагрузок после имплантации зуба, так как это может спровоцировать неблагоприятные последствия в области операции.
- Следите за здоровьем, чтобы не заболеть простудными болезнями. Сбой иммунитета и синдромы, которые сопутствуют ему, такие как кашель, чихание и высокая температура могут спровоцировать отторжение имплантата.
Побочные действия препаратов Нимесил и Кеторол
Нимесил может редко вызывать анемию, геморрагию, панцитопению. Возможны аллергические реакции: зуд, кожные высыпания, покраснение кожных покровов, повышенное выделение слизи и пота. Изредка наблюдаются головокружения, тревожность, ночные кошмары, головные боли, сонливость. Возможно снижение остроты зрения, повышение артериального давления, ускорение сердцебиения. Могут наблюдаться диарея, тошнота, рвота, реже – запоры, метеоризм. Более редки гастриты, образование язвенной болезни. Могут отмечаться примеси крови в моче.
Прием Кеторола может вызвать боли в желудке, диарею, газообразование, запор, рвоту, тошноту, спазмы, гепатит, острую почечную недостаточность, частое мочеиспускание.
Прием Кеторола может вызвать боли в желудке, диарею, газообразование, запор, рвоту, тошноту, спазмы, гепатит, острую почечную недостаточность, частое мочеиспускание, нефрит, нарушение зрения и слуха, ринит, отек гортани, головные боли, головокружение, сонливость, депрессию, галлюцинации, психоз, обмороки, отеки легких, гипертонию, кровотечения из носа, анемию, лейкопению, высыпания на коже, крапивницу, болезненность в месте введения (при инъекциях), отечность, увеличение веса, усиленное выделение пота, отек языка.
Отзывы пациентов
Олег, 34 года, Харьков: «Против болей в пояснице доктор прописал прием Нимесила. Принимал дважды в сутки в течение 10 дней. Состояние сильно улучшилось, исчезли мучительные боли. Сочетал терапию с народными средствами и специальным массажем. Единственный минус – у раствора неприятный кислый привкус».
Елена, 27 лет, Пенза: «Кеторол в таблетках доктора назначили из-за сильной зубной боли, появлявшейся даже в состоянии покоя. Облегчение ощутила уже после первого применения; преимуществом стала и низкая цена лекарства. Пила по 2 таблетки в сутки на протяжение 3 дней. Затем больной зуб пролечили, боли прошли окончательно».
Лекарственные препараты в стоматологической практике. Часть II
В прошлой записи мы с Вами говорили об общих принципах назначения лекарств в амбулаторной стоматологии. Тема еще актуальна, ее можно комментировать и обсуждать.
Сегодня я предлагаю более конкретно рассмотреть обезболивающие и противовоспалительные препараты в стоматологической практике, а в конце этой записи Вас ждет маленький подарок.
Дабы не превращать все это в унылую лекцию по фармакологии, я расскажу Вам только о тех препаратах, которые применяю сам и по которым есть собственные клинические наблюдения.
Attention!
Данная запись — не назначение врача, не рекомендация для пациентов, а простое информационное сообщение, обобщение собственного опыта работы с лекарственными препаратами. Ни в коем случае не принимайте лекарства без назначения врача.
Итак, начнем.
Общие сведения об обезболивающих препаратах.
Все лекарства, которые мы называем «обезболивающими» (анальгетиками), можно разделить на две большие группы.
Первая группа
— наркотические анальгетики: морфин, героин, фентанил, натрия оксибутират и т. д.
Отличительная особенность — влияние, в первую очередь, на центральную нервную систему (ЦНС), отсюда способность купировать даже очень сильные болевые ощущение.
Из минусов — привыкание, седация, психическая или физическая зависимость, угнетение жизненно важных центров ЦНС вплоть до остановки сердца и дыхания.
В амбулаторной стоматологии наркотические анальгетики не применяются. По вполне очевидным причинам — прием наркотиков должен контролироваться врачом.
Вторая группа
— ненаркотические анальгетики: анальгин, ибупрофен, бутадион, нимесулид и т. д.